Cuando hablamos de pH, nos referimos al potencial hidrogeniónico de una solución, es decir, la cantidad de cationes hidronio (H+ o H3O+) que se dispersan en el disolvente de una solución.
Los cationes hidronio son bien conocidos por la definición propuesta por el científico Arhenius por un ácido. Este científico afirma que ácido es cada sustancia capaz de ionizar y producir iones de hidronio en un medio acuoso.
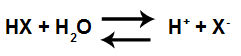
Ecuación de ionización de ácido
el acrónimo pH sirve como referencia para determinar el nivel de acidez de un medio. Pero durante mucho tiempo, los químicos también han utilizado pH como referencia para determinar, además de la acidez, si un medio es básico o neutro.
Esto es posible porque los químicos ahora saben que el agua se autoioniza, es decir, produce hidronios (H+) e hidróxidos (OH-). Así, una solución acuosa nunca tiene solo hidronio o hidróxido, sino ambos, como podemos ver en la siguiente ecuación:

Ecuación de autoionización del agua
Valores utilizados como referencia para el pH
Los valores utilizados para pH se refieren a la constante de ionización (Kw) del agua a una temperatura de 25OC, que es igual a 10-14. A esta temperatura, las concentraciones de iones hidronio e hidróxido producidos por el agua son absolutamente iguales, es decir, 10-7 prostituta.
[H+] = [OH-]= 10-7
A partir de esta referencia, los valores utilizados para el pH oscilan entre 0 y 14.
Fórmulas para calcular el pH
a) Cálculo a partir de la concentración en mol / L de cationes hidronio
El cálculo del valor de pH se puede hacer directamente, siempre que sepamos la concentración de hidronios ([H+]). Vea:
pH = -log [H+]
o
10-pH = [H+]
b) Cálculo a partir de la concentración de aniones hidróxido (OH-)
pOH = -log [OH-]
o
10-pOH = [OH-]
Después de calcular el valor de pOH, debe usarlo en la siguiente expresión para determinar el valor de pH.
pH + pOH = 14
Interpretación de los valores de pH
Conociendo el valor del pH, podemos determinar si la solución en cuestión tiene un carácter ácido, básico o neutro. Para ello, utilice la siguiente relación esquemática:
Para valores de pH inferiores a 7 = medio ácido;
Para pH con un valor igual a 7 = medio neutro;
Para valores de pH superiores a 7 = medio básico.
Ejemplos de
1er Ejemplo: Sabiendo que la concentración de cationes hidronio en una solución es 2.10-4 mol / L, ¿cuál debería ser el valor de pH de esta solución?
Para determinar el valor de pH de la solución a partir de la concentración de hidronios (H+), 2.10-4 mol / L, debemos utilizar la siguiente expresión:
pH = -log [H+]
pH = -log [2.10-4 ]
pH = - (log 2 + log 10-4)
pH = -log2 - log10-4
pH = –log 2 - 4.log 10
pH = –0,3 + 4. (1)
pH = -0,3 + 4
pH = 3,7
2do Ejemplo: Una solución formada por un determinado soluto tiene una concentración de iones hidróxido igual a 10-11 prostituta. A partir de esta concentración, podemos decir que ¿cuánto vale el pH de esta solución?
Para determinar el valor de pH de la solución a partir de la concentración de hidróxido, 10-11 mol / L, debemos hacer lo siguiente:
1O Paso: calcular el valor de pOH.
10-pOH = [OH-]
10-pOH = 10-11
Debemos multiplicar la expresión por -1 porque pOH es siempre una incógnita positiva.
-pOH = -11. (- 1)
pOH = 11
2O Paso: Calcule el valor de pH.
pH + pOH = 14
pH + 11 = 14
pH = 14 - 11
pH = 3
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ph.htm
