Βάση είναι ανόργανη ουσία το οποίο, σύμφωνα με τον Σουηδό χημικό Svante Arrhenius, όταν τοποθετείται σε νερό, υποφέρει το φαινόμενο ιοντική διάσταση, στην οποία υπάρχει η απελευθέρωση του ιόντα: κατιόν (Υ+) και ανιόν υδροξειδίου (ΟΗ-).

Γενικός τύπος βάσης Arrhenius
η ομάδα Υ του α βάση μπορεί να είναι οποιοδήποτε μέταλλο ή αλλιώς της ομάδας αμμωνίου (NH4+), που απελευθερώνονται στο νερό ως κατιόντα κατά τη διάρκεια της αποσύνδεσης, όπως μπορούμε να δούμε στην εξίσωση που αντιπροσωπεύει τη διαδικασία:
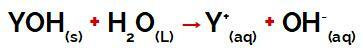
Εξίσωση που αντιπροσωπεύει τη διάσταση μιας βάσης
Δείτε παρακάτω μερικές πολύ σημαντικές πληροφορίες σχετικά με την ταξινόμηση και την ονοματολογία του βάσεις.
1) Ταξινόμηση σχετικά με το διαλυτότητα των βάσεων(ικανότητα να να διαλυθεί μεσα στο ΝΕΡΟ)
Βάσεις διαλυτός: έχουν στη σύνθεση αλκαλικό μέταλλο ή αμμώνιο.
Βάσεις δυσδιάλυτο: έχουν μέταλλο αλκαλικής γαίας στη σύνθεση. Παράδειγμα: υδροξείδιο του μαγνησίου, ευρέως χρησιμοποιούμενο ως αντιόξινο και καθαρτικό.
πρακτικές βάσεις αδιάλυτος: έχετε οποιοδήποτε άλλο μέταλλο στη σύνθεση. Παράδειγμα: υδροξείδιο αργιλίου, ευρέως χρησιμοποιούμενο ως αντιόξινο.
2) Ταξινόμηση σχετικά με το δύναμη βάσης(ικανότητα να διαχωρίζω μεσα στο ΝΕΡΟ)
Βάσεις ισχυρός: έχουν τη σύνθεση μετάλλων αλκαλίων ή αλκαλικών γαιών, με εξαίρεση το μαγνήσιο,
Βάσεις αδύναμος: έχετε οποιοδήποτε άλλο μέταλλο στη σύνθεση.
3) Βασική ονοματολογία
Για να ονομάσετε μια βάση, απλώς ακολουθήστε τον παρακάτω κανόνα ονομασίας:
Υδροξείδιο + de + όνομα μετάλλου ή αμμωνίου
Παράδειγμα: Ca (ΟΗ)2 → υδροξείδιο του ασβεστίου
Εάν η βάση έχει ένα χημικό στοιχείο που δεν ανήκει στις οικογένειες IA, IIA ή IIIA (και αυτό δεν είναι ασημί ή ψευδάργυρο), πρέπει να αναφέρουμε μπροστά από το όνομα του στοιχείου, σε λατινικούς αριθμούς, τον αριθμό του υδροξυλ:
Παράδειγμα: Ti (ΟΗ)4 → υδροξείδιο τιτανίου IV
Από μένα. Diogo Lopes
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-base.htm