Τα αλκένια ή τα αλκένια είναι υδρογονάνθρακες που έχουν διπλό δεσμό στην αλυσίδα του άνθρακα.
Ο γενικός τύπος για τα αλκένια είναι: CόχιΗ2η.
Τα περισσότερα αλκένια παράγονται στο εργαστήριο και λίγα βρίσκονται στη φύση.
Χαρακτηριστικά
Τα κύρια χαρακτηριστικά των αλκενίων είναι:
- άχρωμος
- Αδιάλυτο στο νερό
- Διαλυτό σε αλκοόλη και αιθέρα
- Είναι πιο αντιδραστικά από τα αλκάνια
- Τα σημεία τήξεως και βρασμού είναι υψηλότερα από αυτά των αλκανίων με τον ίδιο αριθμό ατόμων άνθρακα
- Το απλούστερο αλκένιο είναι το αιθυλένιο ή το αιθυλένιο
Μάθετε επίσης για:
- αλκάνια
- Αλκίνες
- αλκαδιένιο
Ονοματολογία
Τα αλκένια λαμβάνουν την ίδια ονοματολογία με άλλους υδρογονάνθρακες.
PREFIX + INFIX + SUFFIX
Το πρόθεμα υποδεικνύει την ποσότητα άνθρακα στην κύρια αλυσίδα.
Το infix δίνεται από τον όρο "en", που αντιπροσωπεύει τον διπλό δεσμό. Το επίθημα δίνεται με το γράμμα "o", το οποίο δείχνει την ένωση υδρογονάνθρακα.
Έτσι, τα αλκένια ονομάζονται επίθημα –Ενο, που δείχνει τον διπλό δεσμό.
Επιπλέον, πρέπει να αναφέρεται η θέση του διπλού δεσμού. Αυτός ο αριθμός προηγείται του ονόματος του αλκενίου και δείχνει το άτομο άνθρακα από το οποίο αρχίζει η σύνδεση.
Η ανθρακική αλυσίδα αρχίζει να αριθμείται από το πλησιέστερο άκρο του διπλού δεσμού.
Παραδείγματα
Αιθένιο ή αιθυλένιο: CH2 = ΧΗ2
Προπυλένιο ή Προπυλένιο: CH2 = CH - CH3, του οποίου ο ισοδύναμος τύπος γράφεται ως εξής: CH3 - CH = CH2
1-βουτένιο: CH2 = CH - CH2 - CH3
2-βουτένιο: CH3 - CH = CH - CH3
Είναι κοινό για τα αλκένια να εμφανίζονται επίσης ισομερισμός:
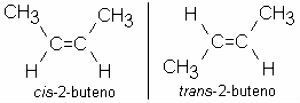
διακλαδισμένα αλκένια
Τα αλκένια μπορούν επίσης να διακλαδίζονται. Σε αυτήν την περίπτωση, η κύρια αλυσίδα είναι η μεγαλύτερη και έχει τον διπλό δεσμό.
Παράδειγμα:
5-μεθυλ-2-εξάνιο
Μάθε περισσότερα για Ονοματολογία υδρογονανθράκων.
Συμπληρώστε την έρευνά σας για Υδρογονάνθρακες. Διαβάστε επίσης:
- Βενζόλιο
- Βουτάνιο
- Κυκλάνοι
- Πετρέλαιο
- ΟΡΓΑΝΙΚΕΣ ΕΝΩΣΕΙΣ
- Αρωματικοί υδρογονάνθρακες
- Ασκήσεις σε Υδρογονάνθρακες