Η επιφανειακή τάση είναι ένα φαινόμενο που εμφανίζεται στην επιφάνεια των υγρών, όπως το νερό, σχηματίζοντας ένα λεπτό υμένιο.
Όταν το νερό, σε υγρή κατάσταση, καταλαμβάνει ένα δοχείο, μπορούμε να αντιληφθούμε τον διαχωρισμό μεταξύ του υγρού και του περιβάλλοντος. Αυτό συμβαίνει επειδή η αλληλεπίδραση μεταξύ των μορίων του νερού στην επιφάνεια είναι διαφορετική από τις αλληλεπιδράσεις στο εσωτερικό του υγρού.
Στην επιφάνεια, ένα μόριο νερού αλληλεπιδρά με μόρια στις πλευρές και κάτω από αυτό. Στο εσωτερικό, ένα μόριο περιβάλλεται από άλλα μόρια και υπάρχει αλληλεπίδραση προς όλες τις κατευθύνσεις μέσω δεσμών υδρογόνου.
Λόγω αυτής της ιδιότητας παρατηρούμε το φαινόμενο του σχηματισμού σταγονιδίων. Εξαιτίας αυτού, είναι επίσης δυνατό για τα έντομα να περπατούν στο νερό.
Τι είναι η επιφανειακή τάση;
Είναι ο σχηματισμός μιας λεπτής μεμβράνης κάτω από ένα υγρό λόγω της ανισότητας έλξης μεταξύ των μορίων που το συνθέτουν. Αυτό το φαινόμενο εμφανίζεται πιο έντονα σε υγρά που έχουν διαμοριακές δυνάμεις έντονο, όπως το νερό.
Οι αλληλεπιδράσεις μεταξύ ειδών σε ένα υγρό ονομάζονται συνεκτικές δυνάμεις. Ενώ τα μόρια μέσα σε ένα υγρό προσελκύονται σε γειτονικά μόρια προς όλες τις κατευθύνσεις, τα μόρια στην επιφάνεια αλληλεπιδρούν με μόρια κάτω και δίπλα τους.
Δείτε πώς εμφανίζεται η επιφανειακή τάση στο νερό.
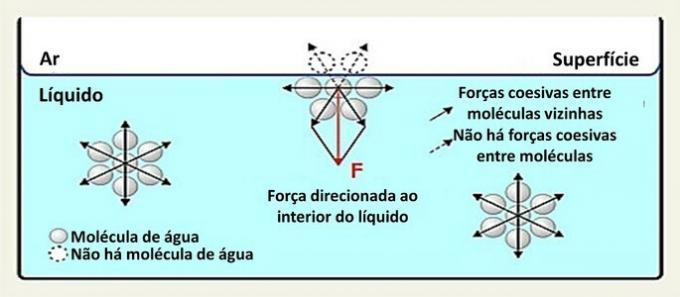
Το νερό (Η2O) είναι ένα πολικό μόριο που σχηματίζεται από 2 άτομα υδρογόνου (θετικοί πόλοι) και ένα άτομο οξυγόνου (αρνητικός πόλος) ομοιοπολικούς δεσμούς. Ο θετικός πόλος ενός μορίου προσελκύεται από τον αρνητικό πόλο του γειτονικού μορίου, σχηματίζοντας δεσμούς υδρογόνου.
Αυτός ο τύπος αλληλεπίδρασης εντός του υγρού κατανέμεται προς όλες τις κατευθύνσεις. Στην επιφάνεια, οι δυνάμεις κατευθύνονται προς τα κάτω και προς τα πλάγια, γιατί πάνω τους δεν υπάρχουν μόρια νερού. Αυτό καθιστά τα επιφανειακά μόρια πιο συνεκτικά και δημιουργεί ένα ελαστικό φιλμ.
Η μονάδα επιφανειακής τάσης δίνεται από το πηλίκο μεταξύ μονάδας δύναμης και μονάδας μήκους, με το πιο υιοθετημένο να είναι dyne / centimeter (dyne / cm) και newton / meter (N / m).
Το νερό έχει υψηλή επιφανειακή τάση, η τιμή του οποίου είναι 72,75 dyne / cm. Ωστόσο, ο υδράργυρος, ένα υγρό μέταλλο, έχει επιφανειακή τάση περίπου 7 φορές μεγαλύτερη από το νερό, 475 dyne / cm.
Θέλετε να μάθετε περισσότερα; Δείτε λοιπόν τα ακόλουθα κείμενα:
- Ιδιότητες νερού
- Πολικά και απολικά μόρια
- Χημικοί δεσμοί
Φαινόμενα που προκαλούνται από επιφανειακή τάση
Η επιφανειακή τάση ευθύνεται για ορισμένα φαινόμενα που παρατηρούμε στην καθημερινή ζωή. Τα κύρια είναι:
Ζώα που περπατούν στο νερό

Τα έντομα, οι αράχνες και άλλα ζώα μπορούν να περπατήσουν ή να ξεκουραστούν στο Νερό γιατί στα άκρα των ποδιών του υπάρχουν τρίχες επικαλυμμένες με λιπαρή ουσία και, ως εκ τούτου, δεν μπορούν να διεισδύσουν μεταξύ των μορίων του νερού που ενώνονται στην επιφάνεια.
Σχηματισμός σταγονιδίων νερού

Τα σταγονίδια νερού είναι σφαιρικά λόγω της συστολής στο μόρια της επιφάνειας που προκαλείται από επιφανειακή τάση. Η σφαίρα εμφανίζεται επειδή αυτό είναι το γεωμετρικό σχήμα στο οποίο υπάρχει η μικρότερη σχέση μεταξύ της επιφάνειας και του όγκου. Επομένως, το σφαιρικό σχήμα διατηρεί τον μικρότερο αριθμό μορίων νερού σε επαφή με τον αέρα.
Ασκήσεις στην επιφανειακή τάση του νερού
1. Ένα επιφανειοδραστικό είναι μια ουσία που δρα σε ένα άλλο για να αλλάξει:
α) Οσμωτικότητα.
β) Επιφανειακή τάση.
γ) Ηλεκτροφόρηση.
δ) Ιξώδες.
ε) Οσμωτική πίεση.
Σωστή εναλλακτική λύση: β) Επιφανειακή τάση.
Α) ΛΑΘΟΣ. Η οσμωτικότητα σχετίζεται με την ποσότητα σωματιδίων διαλυμένης ουσίας που περιέχονται σε δεδομένο όγκο διαλύτη.
β) ΣΩΣΤΗ. Τόσο τα απορρυπαντικά όσο και τα σαπούνια μειώνουν την επιφανειακή τάση του νερού και καλούνται γενικά τασιενεργά, επειδή τα μόρια αυτών των υλικών τοποθετούνται μεταξύ των μορίων νερού και μειώνουν την τάση επιπόλαιος.
γ) ΛΑΘΟΣ. Η ηλεκτροφόρηση είναι μια τεχνική για το διαχωρισμό των μορίων σύμφωνα με τα φορτία τους.
δ) ΛΑΘΟΣ. Το ιξώδες είναι μια φυσική ιδιότητα που καθορίζει την αντίσταση ενός υγρού στη ροή.
ε) ΛΑΘΟΣ. Η οσμωτική πίεση είναι μια συνεργική ιδιότητα που αντιστοιχεί στην πίεση που πρέπει να ασκηθεί σε ένα σύστημα για να αποφευχθεί η αυθόρμητη εμφάνιση όσμωσης.
Μάθετε περισσότερα σχετικά με τα θέματα που καλύπτονται σε αυτό το τεύχος:
- Ιδιότητες υλικού
- Συνεργατικές Ιδιότητες
- Οσμωτική πίεση
2. Η επιφανειακή τάση των υγρών εξαρτάται άμεσα από διεργασίες αλληλεπίδρασης μεταξύ μορίων, όπως η σύνδεση υδρογόνου, για παράδειγμα. Ποια από τις παρακάτω ουσίες έχει την υψηλότερη επιφανειακή τάση;
α) βενζόλιο
β) οκτάνιο
γ) αιθυλική αλκοόλη
δ) τετραχλωριούχος άνθρακας
ε) αιθανοϊκό οξύ
Σωστή εναλλακτική λύση: ε) αιθανοϊκό οξύ.
Α) ΛΑΘΟΣ. Το βενζόλιο είναι ένας υδρογονάνθρακας, ένα μη πολικό μόριο και δεν δημιουργεί δεσμούς υδρογόνου.
β) ΛΑΘΟΣ. Το οκτάνιο είναι ένας υδρογονάνθρακας και, επομένως, είναι ένα μη πολικό μόριο που δεν δημιουργεί δεσμούς υδρογόνου.
γ) ΛΑΘΟΣ. Η αιθυλική αλκοόλη είναι μια ελαφρώς πολική ένωση που μπορεί να σχηματίσει δεσμούς υδρογόνου, αλλά η αλληλεπίδραση μεταξύ των μορίων είναι περιορισμένη.
δ) ΛΑΘΟΣ. Ο τετραχλωράνθρακας είναι μια μη πολική οργανική ένωση και επομένως δεν δημιουργεί δεσμούς υδρογόνου.
ε) ΣΩΣΤΗ. Η λειτουργική ομάδα καρβοξυλικού οξέος (-COOH) μπορεί να δημιουργήσει δεσμούς υδρογόνου είτε με το οξυγόνο είτε με το υδροξύλιο υδρογόνο.

Μάθετε περισσότερα σχετικά με τα θέματα που καλύπτονται σε αυτό το τεύχος:
- Πολικότητα μορίων
- Οργανικές λειτουργίες
- Υδρογονάνθρακες
πείραμα επιφανειακής τάσης
Παρακολουθήστε το παρακάτω βίντεο με ένα πείραμα που δείχνει την επιφανειακή τάση του νερού.