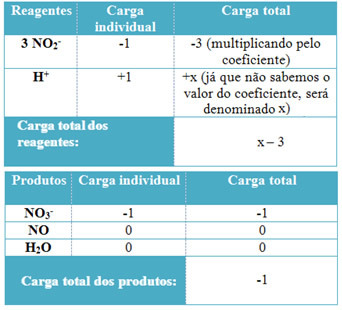
Εξετάστε τη γενική αναστρέψιμη αντίδραση παρακάτω, όπου τα πεζά γράμματα αντιστοιχούν στους ισορροπημένους συντελεστές αντίδρασης και τα κεφαλαία γράμματα είναι τα αντιδρώντα και τα προϊόντα είναι όλα αέρια:

Λαμβάνοντας υπόψη καθεμία από τις οδηγίες αντίδρασης ξεχωριστά, οι ρυθμοί ανάπτυξής τους (Td) δίδονται από:
* Άμεση αντίδραση: aA + bB → cC + dD
Ολααπευθείας = Καπευθείας. [Ο]ο. [ΣΙ]σι
* Αντίστροφη αντίδραση: cC + dD → aA + bB
Ολααντίστροφος = ΚΑΝΤΙΣΤΡΟΦΗ. [ΝΤΟ]ντο. [ΡΕ]ρε
Η σταθερά χημικής ισορροπίας όσον αφορά τη συγκέντρωση στην ποσότητα της ύλης (Κντο) και όσον αφορά τη μερική πίεση (ΚΠ) θα δοθεί διαιρώντας το Καπευθείας από τον ΚΑΝΤΙΣΤΡΟΦΗ.
Έχουμε λοιπόν:
καπευθείας. [Ο]ο. [ΣΙ]σι = 1 → καπευθείας__ = __[ΝΤΟ]ντο. [ΡΕ]ρε___
κΑΝΤΙΣΤΡΟΦΗ. [ΝΤΟ]ντο. [ΡΕ]ρε κΑΝΤΙΣΤΡΟΦΗ [Ο]ο. [ΣΙ]σι
Όντας, Κντο =_Καπευθείας_
κΑΝΤΙΣΤΡΟΦΗ
Έχουμε λοιπόν:
κντο =__[ΝΤΟ]ντο. [ΡΕ]ρε___ ή ΚΠ =__(Πράκα)ντο. (σελ.)ρε___ |
Όπου p είναι η μερική πίεση κάθε ουσίας σε ισορροπία.
Με αυτόν τον τρόπο, κάθε συγκέντρωση αυξάνεται σε έναν εκθέτη που αντιστοιχεί στον συντελεστή της αντίστοιχης ουσίας στην αντίδραση, και Κ
ντο δεν έχει μονάδα *.Επιπλέον, μια πολύ σημαντική πτυχή που πρέπει να επισημανθεί είναι αυτή σε αυτήν την έκφρασηούτε στερεά συστατικά ούτε καθαρά υγρά δεν πρέπει να αντιπροσωπεύονται, καθώς μόνο θέματα που μπορούν να υποστούν παραλλαγή συμμετέχουν σε αυτήν την έκφραση. Η συγκέντρωση στην ποσότητα ύλης μιας ουσίας σε στερεά κατάσταση είναι σταθερή και συνεπώς περιλαμβάνεται ήδη στην τιμή του ίδιου του Κ.ντο. Το ίδιο ισχύει και για καθαρά υγρά όπως το νερό. Εν συντομία, Μόνο ουσίες στην αέρια κατάσταση και σε υδατικό διάλυμα συμμετέχουν στην έκφραση.
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)
Σημειώστε τα παρακάτω παραδείγματα:
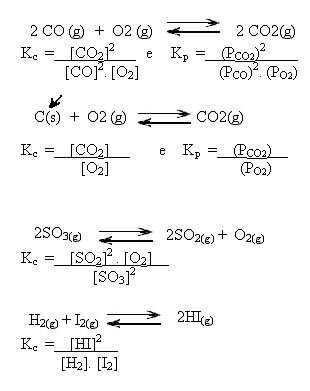
Τιμές Κντο μπορεί να μας δείξει εάν η συγκέντρωση αντιδραστηρίων και προϊόντων είναι ίδια ή εάν το ένα είναι μεγαλύτερο από το άλλο:
- αν κντο ή ΚΠ είναι ίσο με ένα (Κντο = 1)Αυτό σημαίνει ότι η συγκέντρωση των αντιδραστηρίων και των προϊόντων είναι ίση.
- εάν η τιμή του κντο ή ΚΠ να είσαι ψηλός, αυτό σημαίνει ότι τα προϊόντα βρίσκονται σε μεγαλύτερη συγκέντρωση, επειδή στην έκφραση του Κντο τα προϊόντα είναι στον αριθμητή ·
- εάν η τιμή του κντο ή ΚΠ είναι χαμηλό, αυτό σημαίνει ότι τα αντιδραστήρια βρίσκονται σε υψηλότερη συγκέντρωση, επειδή στην έκφραση του Κντο τα αντιδραστήρια βρίσκονται στον παρονομαστή.
*Κντο και ΚΠ Είναι αριθμοί χωρίς διάσταση, δηλαδή, καθαροί αριθμοί, χωρίς μονάδα που σχετίζεται με οποιοδήποτε μέγεθος ή σχέση μεταξύ μεγεθών.
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Σταθερές ισορροπίας Kc και Kp"; Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. Πρόσβαση στις 28 Ιουνίου 2021.