Ο ενέργεια ενεργοποίησης είναι η ελάχιστη ποσότητα ενέργειας που απαιτείται για τη σύγκρουση μεταξύ των σωματιδίων αντιδρώντος, που γίνεται με ευνοϊκό προσανατολισμό, για να πραγματοποιηθεί και να οδηγήσει σε αντίδραση.
Οι αντιδράσεις εμφανίζονται μόνο όταν τα αντιδραστήρια έχουν ενέργεια ενεργοποίησης (ή την ελάχιστη απαιτούμενη ενέργεια, η οποία ποικίλλει από αντίδραση σε αντίδραση. είτε σε ποσότητα είτε σε μορφή) ή όταν τους παρέχεται.
Για παράδειγμα, όταν το μεταλλικό νάτριο έρχεται σε επαφή με νερό, αντιδρά βίαια. Αυτό σημαίνει ότι το ενεργειακό περιεχόμενο αυτών των αντιδραστηρίων είναι ήδη επαρκές για να λάβει χώρα η αντίδραση.
Σε περίπτωση ενεργοποίησης της σόμπας, η αντίδραση καύσης θα συμβεί μόνο εάν τοποθετήσουμε ένα φωτισμένο σπίρτο ή κάποια άλλη πηγή φωτιάς κοντά στο αέριο που απελευθερώνεται από τη σόμπα. Αυτό σημαίνει ότι, στην περίπτωση αυτή, ήταν απαραίτητο να παρέχεται ενέργεια στο σύστημα έτσι ώστε να φτάσει στην ενέργεια ενεργοποίησης και να λάβει χώρα η αντίδραση.
Στην περίπτωση του φωσφόρου που χρησιμοποιείται για την καύση, η ενέργεια ενεργοποίησης παρέχεται με τριβή. Το ίδιο συμβαίνει και με αναπτήρες, οι οποίοι χρειάζονται επίσης ένα σπινθήρα που δίνει την απαραίτητη ενέργεια ενεργοποίησης για την καύση του αερίου που περιέχεται σε αυτά.
Η ενέργεια ενεργοποίησης μπορεί επίσης να παρέχεται από το φως, όπως συμβαίνει με την αποσύνθεση του υπεροξειδίου του υδρογόνου. Γι 'αυτό αποθηκεύεται σε σκούρα ή αδιαφανή μπουκάλια.
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)

Έτσι, μπορούμε να συμπεράνουμε ότι η ενέργεια ενεργοποίησης (Εμέχρι) είναι η διαφορά μεταξύ της ενέργειας που απαιτείται για την έναρξη της αντίδρασης (Ε) και της ενέργειας που περιέχεται στα αντιδραστήρια (Επρ):

Η ενέργεια ενεργοποίησης είναι ένα εμπόδιο για να λάβει χώρα η αντίδραση και είναι απαραίτητη για τη διάσπαση των δεσμών των αντιδρώντων. Με αυτό, λαμβάνει χώρα η αντίδραση και γίνονται νέες συνδέσεις για τον σχηματισμό των προϊόντων.
Όταν η σύγκρουση μεταξύ σωματιδίων αντιδραστηρίων με ευνοϊκό προσανατολισμό συμβαίνει με ίση ενέργεια ή υψηλότερη από την ενέργεια ενεργοποίησης, πριν από το σχηματισμό των προϊόντων, σχηματίζεται μια ενδιάμεση και ασταθής κατάσταση, εκφρασμένο ενεργοποιήθηκε το σύμπλεγμα, στον οποίο οι αντιδρώντες δεσμοί αποδυναμώνουν και σχηματίζονται οι δεσμοί προϊόντος. Ετσι, η ενέργεια ενεργοποίησης είναι η ενέργεια που απαιτείται για το σχηματισμό του ενεργοποιημένου συμπλόκου.
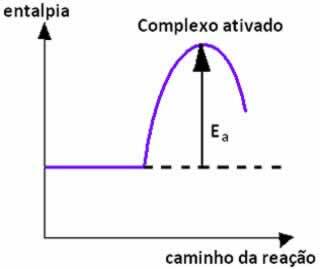
Παρακάτω έχουμε ένα γράφημα που δείχνει την ενέργεια ενεργοποίησης ως εμπόδιο για την πραγματοποίηση της αντίδρασης:
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Ενέργεια ενεργοποίησης"; Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/energia-ativacao.htm. Πρόσβαση στις 27 Ιουνίου 2021.