Sulfonierungsreaktionen in Alkanen Sie sind organische Substitutionsreaktionen, durchgeführt mit dem Ziel der Herstellung Sulfonsäuren (organische Verbindungen mit der SO-Gruppe3H an ein Kohlenstoffatom oder eine Kohlenstoffkette gebunden) und Wasser (H2Ö).
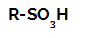
Strukturformel einer Sulfonsäure
Zur Durchführung einer Sulfonierungsreaktion an alkane, müssen wir ein Alkan (eine Verbindung, die aus einer Kohlenstoffkette besteht, die nur mit Kohlenstoff- und Wasserstoffatomen gesättigt ist) und die Schwefelsäure (H2NUR4) konzentriert, erhitzt (∆).
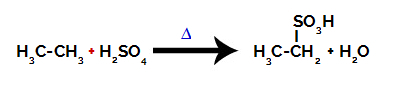
Chemische Gleichung, die die Sulfonierung eines Zwei-Kohlenstoff-Alkans darstellt
Prinzipien der Sulfonierungsreaktion in Alkanen
Sowie Alkansulfonierungsreaktion es ist eine Substitutionsreaktion, wir haben darin einen Austausch zwischen kleineren Komponenten Elektronegativität der Reaktanten, also zwischen Alkan und Schwefelsäure. Alkan hat Wasserstoff und Schwefelsäure die Sulfonsäuregruppe.
Unten haben wir den Schritt für Schritt des Mechanismus von a Sulfonierungsreaktion in Alkanen. Als Beispiel verwenden wir das einfachste Alkan, Methan (CH4):
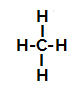
Strukturformel von Methan
1. Schritt: Aufbrechen der Bindung zwischen Hydroxyl (OH) und Schwefel (S) in Schwefelsäure.
Jede in Schwefelsäure vorhandene Hydroxylgruppe ist dadurch gekennzeichnet, dass sie elektronegativer ist. Beim Erhitzen während der Reaktion besteht die Tendenz, dass die Bindung zwischen der Hydroxylgruppe und dem Schwefel gebrochen wird:
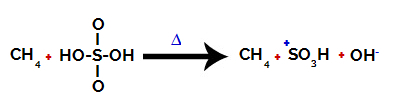
Unterbrechung der Bindung zwischen Schwefel und Hydroxyl
Das Aufbrechen der Bindung aller Hydroxyle kommt jedoch wegen der elektronischen Umlagerung in der Struktur nicht vor. Dann wird ein Hydroxid-Anion (OH) erhalten.-) und ein Sulfonsäurekation.
2. Schritt: Angriff der Hydroxylgruppe auf das Alkanmolekül.
Dann wird die Hydroxygruppe (OH-) führt einen Angriff auf das Alkan aus, wodurch die Bindung zwischen Kohlenstoff und Wasserstoff (die aufgrund der unterschiedlichen Elektronegativität zwischen ihnen brüchiger ist) gebrochen wird.
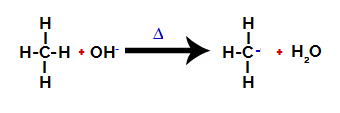
Aufbrechen der Bindung zwischen Kohlenstoff und Wasserstoff in Alkanen
Hinweis: Eine Unterbrechung der Bindung zwischen Kohlenstoff und Wasserstoff tritt immer am häufigsten auf Kohlenstoff mit geringerer Elektronendichte oder Ladung auf. Je weniger Wasserstoffatome Kohlenstoff aufweist oder je mehr Gruppen daran gebunden sind, desto geringer ist seine Elektronendichte. Also haben wir:
Tertiärer Kohlenstoff < Sekundärer Kohlenstoff < Primärer Kohlenstoff
Nach dem Aufbrechen der Bindung wird das Alkan zu einem elektronenarmen Kohlenstoff (Carbokation). Die Hydroxidgruppe (OH)-) wechselwirkt mit dem freigesetzten Wasserstoff und bildet ein Wassermolekül.
3. Schritt: Angriff des gebildeten Radikals an der Sulfonsäuregruppe.
Schließlich wird die Sulfonsäuregruppe vom Rest des Alkans angegriffen, wodurch eine Sulfonsäure entsteht.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
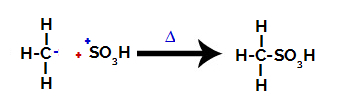
Strukturen, die interagieren und Sulfonsäure bilden
Beispiele für Gleichungen, die Sulfonierungsreaktionen in Alkanen darstellen
1. Beispiel: Sulfonierung von Propan.
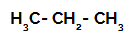
Strukturformel von Propan
Propan hat zwei primäre Kohlenstoffe und einen sekundären Kohlenstoff, die unterschiedliche Ladungen haben, weil sie an unterschiedliche Mengen an Wasserstoff gebunden sind. Da Kohlenstoff elektronegativer ist als Wasserstoff, haben diese Kohlenstoffe unterschiedliche Elektronendichten.
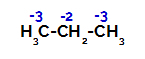
Ladungsverteilung an jedem Kohlenstoffatom von Propan
An primären Kohlenstoffen beträgt die Ladung -3 (weil er an drei Wasserstoffatome gebunden ist) und am sekundären Kohlenstoff beträgt die Ladung -2 (weil er an zwei Wasserstoffatome gebunden ist). So kommt es zu einer Unterbrechung der Bindung zwischen Kohlenstoff und Wasserstoff, manchmal an Kohlenstoff 1 (eines Moleküls), manchmal an Kohlenstoff 2 (eines anderen Moleküls).
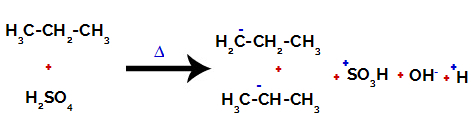
Aufbrechen der Bindung zwischen Kohlenstoff und Wasserstoff an verschiedenen Kohlenstoffen
Nach den Brüchen zwischen den Bindungen, sowohl in Schwefelsäure als auch in Alkanen, kommt es zur Bildung von Produkte mit dem Ersatz von Wasserstoff an Kohlenstoff 1 durch eine Sulfongruppe, und das gleiche geschieht an Kohlenstoff 2.
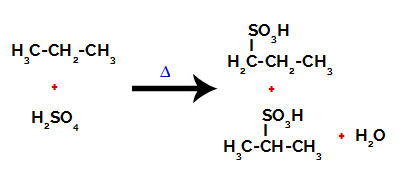
Produkte aus der Sulfonierung von Propan
2. Beispiel: Sulfonierung von 2-Methyl-butan.

Strukturformel von 2-Methyl-Butan
2-Methyl-Butan hat drei primäre Kohlenstoffe, einen sekundären Kohlenstoff und einen tertiären Kohlenstoff, die unterschiedliche Ladungen und damit unterschiedliche elektronische Dichten, wie in der folgenden Struktur zu sehen ist:
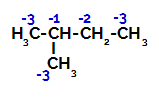
Verteilung elektronischer Ladungen in 2-Methyl-Butan
Daher gibt es in 2-Methyl-Butan mehrere Möglichkeiten, die Bindung zwischen Kohlenstoff und Wasserstoff zu brechen, die an Kohlenstoff 1 (eines Moleküls), Kohlenstoff 2 (eines anderen Moleküls), Kohlenstoff 3 oder Kohlenstoff auftreten können 4. Es ist jedoch bemerkenswert, dass die Störung bei Kohlenstoff Nummer 2 häufiger vorkommt.
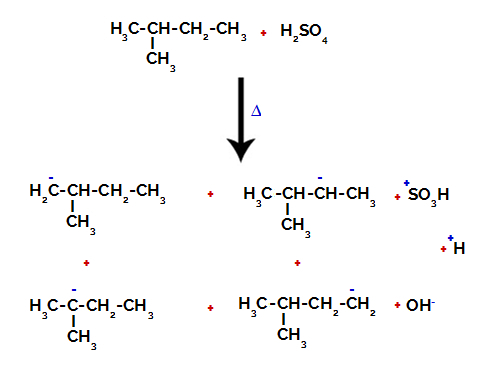
Aufbrechen der Bindung zwischen Kohlenstoff und Wasserstoff an verschiedenen Kohlenstoffen
Nach dem Bruch zwischen den Bindungen, sowohl in Schwefelsäure als auch in Alkanen, bildet sich Produkte mit dem Ersatz des Wasserstoffs an Kohlenstoff 1 durch eine Sulfonsäuregruppe, und das gleiche geschieht an der Kohlenstoff 2.

Produkte aus der Sulfonierung von 2-Methyl-butan
Von mir. Diogo Lopes Dias
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
TAGE, Diogo Lopes. "Sulfonierungsreaktionen in Alkanen"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/reacoes-sulfonacao-alcanos.htm. Zugriff am 28. Juni 2021.