Wasser allein kann kein Fett aus Materialien entfernen. Das ist weil DasWasser ist polar, wie in der Abbildung unten gezeigt, aufgrund des Unterschieds in der Elektronegativität, der zwischen den Wasserstoff- und Sauerstoffatomen ihrer Moleküle besteht. Andererseits, das Fett ist unpolar und daher löst Wasser keine Fette.
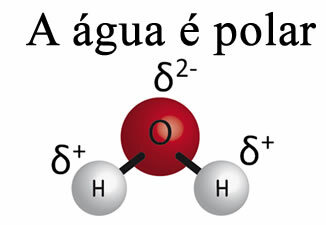
Außerdem hat Wasser etwas namens oberflächliche Spannung. Im Text kann man das besser verstehen. Oberflächenspannung von Wasser, aber im Grunde ist es eine Art elastischer Film oder eine Membran, die sich auf der Wasseroberfläche bildet, die verhindert, dass Stoffe und andere Materialien durchdringen, um Schmutz zu entfernen. Wassermoleküle ziehen sich in alle Richtungen durch Wasserstoffbrücken, aber Oberflächenmoleküle interagieren nur mit Molekülen an der Seite und unten, wodurch ein Unterschied in Kohäsionskräfte, wodurch sich die Oberflächenmoleküle zusammenziehen und diese Oberflächenspannung bilden.
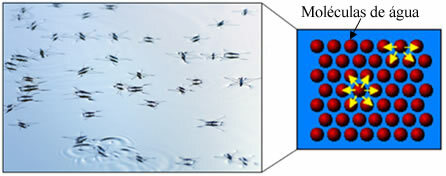
Hier kommen Seifen und Waschmittel ins Spiel (aus dem Lateinischen
entgiften = klar), die auch genannt werden Tenside, da sie die Oberflächenspannung von Wasser reduzieren und zudem mit Wasser und Fett interagieren. Wie kommt es dazu?Seifen und Waschmittel enthalten Fettsäuresalze, bei denen es sich um lange Moleküle handelt, die von a. gebildet werden unpolarer Teil (was ist hydrophob – Wasserkraft = Wasser; Phoben = Abneigung) und a polares Ende (hydrophil – Wasserkraft = Wasser; Stamm = Freund). Unten haben wir eine typische Struktur einer Seife:
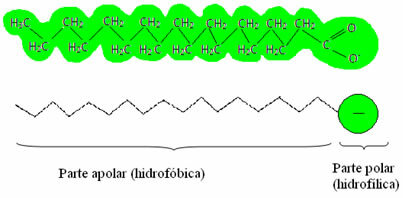
Im Allgemeinen sind Detergenzien Salze von langkettigen Sulfonsäuren:
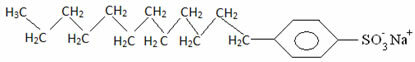
So interagiert der unpolare Teil dieser Moleküle in Seifen und Waschmitteln mit dem Fett, während das polare Ende mit Wasser interagiert und sich in kleine Kügelchen gruppiert, angerufen von Mizellen, bei der die hydrophilen Teile in Kontakt mit den Wassermolekülen zur Außenseite der Mizelle zeigen, und die Fett bleibt auf der Innenseite, in Kontakt mit dem unpolaren oder hydrophoben Teil, ein Prozess ähnlich dem im Bild a Folgen:
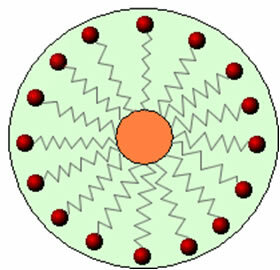
Auf diese Weise wird der fettige Schmutz in der Mitte der Mizellen eingeschlossen und kann entfernt werden. Ein weiterer Punkt ist, dass Waschmittel und Seifen die Oberflächenspannung von Wasser senken können, weil verringern die Wechselwirkungen zwischen seinen Molekülen, wodurch es einfacher wird, verschiedene Materialien zu durchdringen, um die Schmutz.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/quimica-dos-saboes-detergentes.htm

