Lernen Sie, den ersten Hauptsatz der Thermodynamik in verschiedenen Situationen anzuwenden, lösen Sie Aufgaben und testen Sie Ihr Wissen anhand gelöster und erklärter Aufgaben.
Frage 1
Der erste Hauptsatz der Thermodynamik besagt:
a) Energie kann nicht erzeugt oder zerstört werden, sie kann jedoch von einer Form in eine andere umgewandelt werden.
b) Energie bleibt immer erhalten, kann aber nicht von einer Form in eine andere umgewandelt werden.
c) Energie kann erzeugt oder zerstört werden, sie kann jedoch nicht von einer Form in eine andere umgewandelt werden.
d) Energie kann nicht konserviert, aber von einer Form in eine andere umgewandelt werden.
Der erste Hauptsatz der Thermodynamik ist der Grundsatz der Energieerhaltung, also in einem System Im geschlossenen Zustand bleibt die Energiemenge konstant und kann nur von einer Form in eine andere umgewandelt werden. andere.
Frage 2
Gehen Sie von einem geschlossenen System aus, das 100 J Wärme aufnimmt und dabei 50 J Arbeit verrichtet. Wie groß ist die Veränderung der inneren Energie des Systems?
a) -50 J
b) 0J
c) 50 J
d) 100J
e) 150J
Kontrolle der Schilder:
Die empfangene Wärme ist positiv Q > 0.
Die geleistete Arbeit ist positiv W > 0.
Nach dem ersten Gesetz gilt:
Frage 3
Ein ideales Gassystem tauscht 500 Joule Wärme mit der Außenumgebung aus. Unter der Annahme, dass es sich bei diesem Prozess um eine isometrische Abkühlung handelt, bestimmen Sie die Arbeit bzw. die innere Energie.
a) 500 J und 0 J
b) - 500 und 0 J
c) 0 J und 500 J
d) 0 J und - 500 J
e) -500 J und 500 J
Da der Prozess isometrisch ist, ändert sich das Volumen nicht, die Arbeit ist also Null.
Nach dem ersten Hauptsatz der Thermodynamik:
Da es sich um eine Kühlung handelt, verliert das System Wärme, daher:
Frage 4
8 Mol eines idealen Gases werden in einem Kolben-Zylinder-System durch 1000 J Arbeit komprimiert. Dabei gehen 400 J Wärme an die äußere Umgebung verloren. Seine innere Energie und die Änderung seiner Temperatur sind jeweils gleich
Gegeben: R = 8,31 J/mol. K
a) - 1400 J und ungefähre Variation von 6 K
b) 600 J und ungefähre Variation von 6 K
c) 600 J und ungefähre Variation von 14 K
d) - 1400 J und ungefähre Variation von 14 K
innere Energie
Wenn das System Arbeit aufnimmt, ist sein Vorzeichen negativ, ebenso wie die Wärme, die bei diesem Prozess verloren geht.
Der erste Hauptsatz der Thermodynamik lautet:
Wenn wir die Werte ersetzen, erhalten wir:
R = 8,31 J/mol K
Temperatur
Nach dem Jouleschen Gesetz gilt:
Frage 5
Ein perfektes Gas wird komprimiert und leistet dabei eine Arbeit von 500 J. Am Ende dieser Transformation änderte sich die innere Energie des Systems um 200 J weniger als zu Beginn. Die vom Gas ausgetauschte Wärmemenge betrug
a) - 700 J
b) - 300 J
c) 300J
d) 0J
e) 700 J
Da es sich um eine empfangene, also widerständige Arbeit handelt, ist ihr Vorzeichen negativ.
Einsetzen der Werte in die Gleichung des ersten Hauptsatzes der Thermodynamik:
Frage 6
(CEDERJ 2021) In einer Phase des Zyklus, der von einem idealen Gas in einer Klimaanlage ausgeführt wird, wird der Gasdruck erhöht, wobei sein Volumen konstant bleibt. In diesem Stadium des Zyklus betragen die vom Gas geleistete Arbeit W, die von ihm absorbierte Wärmemenge Q und die Änderung ΔT seiner Temperatur jeweils:
a) W < 0, Q < 0 und ΔT < 0
b) W = 0, Q > 0 und ΔT > 0
c) W = 0, Q = 0 und ΔT = 0
d) W > 0, Q > 0 und ΔT > 0
Daten:
Druck P steigt;
Das Volumen bleibt konstant;
Arbeiten
Da das Volumen konstant ist, ist die Arbeit W gleich Null.
Der erste Hauptsatz der Thermodynamik lautet wie folgt:
Da Wärme positiv ist, wird auch die Veränderung der inneren Energie positiv sein.
Hitze
Da Wärme absorbiert wird, ist sie positiv.
Temperatur
Nach dem Gasgesetz:
Wo,
n ist die Anzahl der Mol
R ist die universelle Gaskonstante
Somit hängt die Temperatur nur vom Druck ab, da das Volumen konstant und positiv ist.
Frage 7
(UNICENTRO 2018) Nach dem ersten Hauptsatz der Thermodynamik beträgt die Änderung der inneren Energie eines Systems, ΔU gegeben durch die Differenz zwischen der mit der Außenumgebung ausgetauschten Wärme Q und der dabei geleisteten Arbeit W thermodynamisch. Unter Berücksichtigung dieser Informationen kann diese Umwandlung durch die Gleichung dargestellt werden, wenn sich ein einatomiges Gas so ausdehnt, dass es immer die gleiche Temperatur behält
a) ΔU + W = 0
b) ΔU − W =0
c) Q − W = 0
d) Q + ΔU = 0
Der isotherme Prozess erfolgt ohne Temperaturänderung.
Energie hängt mit der Temperatur zusammen:
Dabei ist n die Anzahl der Mol und R die universelle Gaskonstante. Da n und R konstant sind, gibt es nur Temperaturschwankungen und
Der erste Hauptsatz der Thermodynamik lautet wie folgt:
Frage 8
(URCA 2016) Gemäß dem ersten Hauptsatz der Thermodynamik, wenn während eines isothermen Prozesses, den ein ideales Gas fester Masse durchläuft, das Gas freigesetzt wird eine Wärmemenge, deren Größe 50 cal beträgt, dann sind die Änderung der inneren Energie und die vom Gas in diesem Prozess geleistete Arbeit: bzw:
a) 0 und 50 Kal.
b) 50 cal und 0.
c) 0 und 0.
d) 50 Kal. und -50 Kal.
e) 0 und -50 Kal.
Die Änderung der inneren Energie steht in direktem Zusammenhang mit der Temperaturänderung. Da der Prozess isotherm ist, gibt es keine Temperaturänderung .
Aus dem ersten Hauptsatz der Thermodynamik:
Da Wärme freigesetzt wird, ist ihr Vorzeichen negativ.
Frage 9
(UFRN 2012) Biomasse ist eine der Hauptquellen erneuerbarer Energie und daher sind Maschinen, die sie als Brennstoff zur Stromerzeugung nutzen, aus ökologischer Sicht wichtig. Ein sehr häufiges Beispiel ist die Nutzung von Biomasse zum Antrieb einer Dampfturbine zur Arbeitserzeugung. Die nebenstehende Abbildung zeigt schematisch ein vereinfachtes thermoelektrisches Kraftwerk.
In diesem thermoelektrischen Kraftwerk entsteht durch die Verbrennung von Biomasse im Ofen Wärme, die das Wasser im Kessel erhitzt und Hochdruckdampf erzeugt. Der Dampf wiederum wird durch Rohre zur Turbine geleitet, die unter ihrer Einwirkung beginnt, ihre Schaufeln zu drehen.
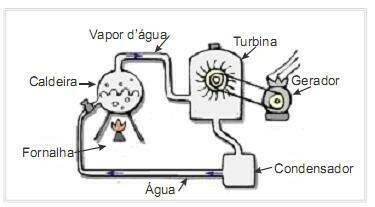
Gehen Sie davon aus, dass Wärmeverluste aufgrund von Temperaturunterschieden zwischen den Teilen dieser Wärmekraftmaschine und der Umgebung vernachlässigbar sind. In diesem Zusammenhang die Variation der inneren Energie des Kesselwassers
a) ist größer als die Summe der ihr durch die Verbrennung der Biomasse zugeführten Wärme und der an der Turbine geleisteten Arbeit.
b) ist gleich der Summe der ihm durch die Verbrennung der Biomasse zugeführten Wärme und der an der Turbine geleisteten Arbeit.
c) ist gleich der Differenz zwischen der ihr durch die Verbrennung der Biomasse zugeführten Wärme und der an der Turbine geleisteten Arbeit.
d) größer ist als die Differenz zwischen der ihr durch die Verbrennung der Biomasse zugeführten Wärme und der an der Turbine geleisteten Arbeit.
Das Wasser im Kessel erhält Energie in Form von Wärme durch die Verbrennung des Brennstoffs und gibt Energie in Form von an der Turbine verrichteter Arbeit ab.
Frage 10
(UECE 2021) Bezüglich der Eigenschaften von Gasen sind folgende Aussagen zu beachten:
ich. Bei einem idealen Gas ist die innere Energie nur eine Funktion des Drucks.
II. Die von einem Gas bei der Zustandsänderung aufgenommene Wärme ist prozessunabhängig.
III. Die innere Energie eines idealen Gases ist nur eine Funktion der Temperatur und unabhängig vom Prozess.
IV. Bei der isothermen Expansion eines idealen Gases ist die von ihm geleistete Arbeit gleich der aufgenommenen Wärme.
Es ist richtig, was nur darin steht
a) I und II.
b) III und IV.
c) I und IV.
d) II und III.
III. RICHTIG. Die innere Energie eines idealen Gases ist nur eine Funktion der Temperatur und unabhängig vom Prozess.
Die Änderung der inneren Energie steht in direktem Zusammenhang mit der Temperaturänderung.
Dabei ist n die Anzahl der Mol und R die ideale Gaskonstante. Da es sich um Konstanten handelt, bestimmt nur die Temperatur die innere Energie des Gases.
IV. RICHTIG. Bei der isothermen Expansion eines idealen Gases ist die von ihm geleistete Arbeit gleich der aufgenommenen Wärme.
Da es isotherm ist, gibt es keine Temperaturänderung, sodass die Änderung der inneren Energie Null ist. Nach dem ersten Hauptsatz der Thermodynamik:
Erfahren Sie mehr mit:
- Erster Hauptsatz der Thermodynamik
- Thermodynamik: Gesetze, Konzepte, Formeln und Übungen
- Übungen zur Thermodynamik
- Gasgesetz
ASTH, Rafael. Übungen zum ersten Hauptsatz der Thermodynamik.Alles zählt, [n.d.]. Verfügbar in: https://www.todamateria.com.br/exercicios-da-primeira-lei-da-termodinamica/. Zugang unter:
Auch sehen
- Übungen zur Thermodynamik
- Thermodynamik
- adiabatische Transformation
- Übungen zur Thermochemie
- Erster Hauptsatz der Thermodynamik
- Naturwissenschaften und ihre Technologien: Enem
- Wärmeenergie
- Zweiter Hauptsatz der Thermodynamik