Der pH-Wert entspricht dem Wasserstoffpotential einer Lösung. Sie wird durch die Konzentration der Wasserstoffionen (H+) und dient zur Messung des Säure-, Neutral- oder Alkalitätsgrades einer gegebenen Lösung.
Neben dem pH-Wert gibt es noch eine weitere Größe, die den Säure- und Basizitätsgehalt eines wässrigen Systems bestimmt: der pH-Wert (Hydroxylion-Potential). Diese Skala hat die gleiche Funktion wie der pH-Wert, wird jedoch weniger verwendet.
pH-Skala
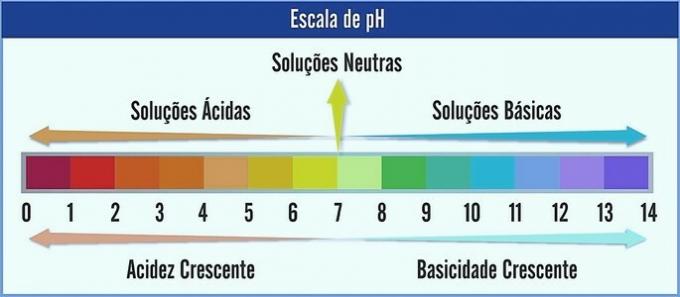
Der pH-Wert wird auf einer Skala von 0 bis 14 dargestellt. Es misst den Säure- und Basizitätsgehalt einer Lösung.
Daher stellt pH 7 eine neutrale Lösung dar (zB reines Wasser). Diejenigen, die davor stehen, gelten als saure Lösungen (saurer pH-Wert), und diejenigen nach 7 sind die basischen Lösungen (alkalischer pH-Wert).
Bei dieser Beobachtung nimmt der Säurecharakter von rechts nach links zu. Der Grundcharakter, von links nach rechts. Beachten Sie, dass die Lösung umso saurer ist, je niedriger der pH-Wert ist.
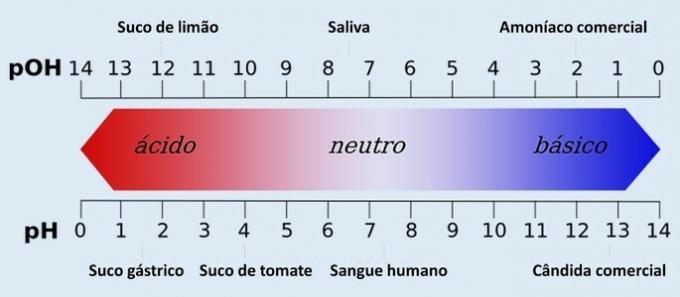
Erfahren Sie mehr unter:
- Pufferlösung
- Titration
- Neutralisierungsreaktion
Beispiele
Säurelösungen
| Lösung | pH |
|---|---|
| Magensäure | 2,0 |
| Zitronensaft | 2,2 |
| Essig | 3,0 |
| Kaffee | 5,0 |
| Kuhmilch | 6,4 |
Basislösungen
| Lösung | pH |
|---|---|
| Menschen Blut | 7,35 |
| Meerwasser | 7,4 |
| Natriumbicarbonat | 8,4 |
| Magnesiamilch | 10,5 |
| Bleichen | 12,5 |
Wie berechnet man den pH-Wert?
1909 schlug der dänische Chemiker Soren Sörensen (1868-1939) vor, dass der Säuregehalt von Lösungen, gemessen an der Konzentration von H-Ionen+, seine Werte mit Hilfe von Logarithmen transformiert, um das Verständnis zu erleichtern.
Bei einer Temperatur von 25 °C beträgt das ionische Produkt von Wasser 10–14 mol2/L2.
Wenn wir den Kologarithmus im Ausdruck anwenden, müssen wir:
Durch diesen Ausdruck können wir den entsprechenden Wert von einer Skala zur anderen durch Subtraktion erhalten.
Wie misst man den pH-Wert?
Die Kontrolle des pH-Wertes ist nicht nur für wissenschaftliche Zwecke wichtig, sondern auch im Alltag.
Der pH-Wert des Pools muss überprüft werden, ebenso wie der pH-Wert des Aquariums und sogar der pH-Wert des Bodens, um bestimmte Pflanzenarten zu berücksichtigen.
Nachfolgend finden Sie die wichtigsten Methoden zur Messung des pH-Werts.
Säure-Basen-Indikator
Um den pH-Wert einer Lösung zu messen, werden sogenannte Säure-Basen-Indikatoren verwendet. Es handelt sich um Substanzen, die ihre Farbe ändern und den Charakter der Lösung anzeigen. Die am häufigsten verwendeten Indikatoren sind: Lackmus und Phenolphthalein.

Schrittzähler
Zusätzlich zu Indikatoren kann der pH-Wert einer Lösung mit einem Instrument namens Peagometer gemessen werden. Dieses elektronische Gerät misst die elektrische Leitfähigkeit der Lösung und wandelt sie in die pH-Wert-Skala um.

Aufnahmeprüfungsübungen mit Feedback
1. (Enem/2014) Ein Forscher stellt fest, dass das Etikett eines der Gläser, in denen er ein Konzentrat von Verdauungsenzymen aufbewahrt, unleserlich ist. Er weiß nicht, welches Enzym das Glas enthält, vermutet aber, dass es sich um eine Magenprotease handelt, die im Magen arbeitet, indem sie Proteine verdaut.
Da er weiß, dass die Verdauung im Magen sauer und der Darm basisch ist, stellt er fünf Reagenzgläser mit Nahrung zusammen anders, das Enzymkonzentrat zu Lösungen mit einem bestimmten pH-Wert geben und abwarten, ob das Enzym in irgendeiner ihr.
Das Reagenzglas, in dem das Enzym wirken muss, um anzuzeigen, dass die Hypothese des Forschers richtig ist, enthält:
a) Kartoffelwürfel in Lösung mit pH = 9
b) Stück Fleisch in Lösung mit pH = 5
c) gekochtes Eiweiß in Lösung mit pH = 9
d) Portion Nudeln in Lösung mit pH = 5
e) Butterkugel in Lösung mit pH = 9
Richtige Alternative: b) Stück Fleisch in Lösung mit pH = 5.
Protease ist ein Enzym, das Proteine verdaut und, da es im Magen ist, im Magen wirkt, dessen pH-Wert sauer ist.
Bei der Analyse der Alternativen müssen wir:
eine falsche. Kartoffeln sind reich an Kohlenhydraten und der pH-Wert des Konzentrats ist basisch.
b) RICHTIG. Fleisch enthält Proteine und Enzyme können darauf einwirken, und der pH-Wert des Konzentrats ist wie im Magen sauer.
c) FALSCH. Der pH-Wert des Konzentrats ist basisch.
d) FALSCH. Nudeln sind reich an Kohlenhydraten.
e) FALSCH. Der pH-Wert des Konzentrats ist basisch.
2. (Udesc/2009) "Saurer Regen" ist ein Begriff, der sich auf Niederschläge aus der Regenatmosphäre mit überdurchschnittlich hohen Mengen an Salpeter- und Schwefelsäure bezieht.
Die Vorläufer des sauren Regens stammen sowohl aus natürlichen Quellen wie Vulkanen und verfallender Vegetation als auch aus Prozessen Industrieemissionen, hauptsächlich Schwefeldioxid und Stickoxide aus der Verbrennung von Kraftstoffen Fossilien.
Der pH-Wert von Regenwasser, der als normal angesehen wird, beträgt 5,5 (aufgrund des Vorhandenseins von Kohlensäure aus der Solubilisierung von Kohlendioxid). Ein Chemiker, der eine hochindustrialisierte Region überwachte, stellte fest, dass der pH-Wert von Regenwasser 4,5 betrug.
Wenn man bedenkt, dass der Säuregehalt mit der H-Konzentration zusammenhängt3Ö+, ist es richtig zu sagen, dass Wasser mit pH 4,5 war:
a) doppelt so basisch wie normal.
b) doppelt so sauer wie normal.
c) zehnmal basischer als normal.
d) zehnmal saurer als normal.
e) hundertmal saurer als normal.
Richtige Alternative: d) zehnmal saurer als normal.
Nach den Ausdrücken pH = - log [H+] und [H+] = 10-pH, Wir müssen:
pH = 5,5
[H+] = 10-5,5
pH = 4,5
[H+] = 10-4,5
Der Unterschied zwischen den Werten beträgt: 10- 5,5 - ( - 4,5) = 10 -1
Da die pH-Skala eine logarithmische Skala ist, entspricht eine Änderung einer Einheit einer 10-fach saureren Lösung.
3. (UFMG/2009) Betrachten Sie eine bestimmte Menge Wasser und Zitronensaft, gemischt, in einem Glas enthalten. Überprüfen Sie diese drei Aussagen zu diesem System:
ICH. Das System ist sauer.
II. Der pH-Wert des Systems ist größer als 7.
III. Im System ist die Konzentration der H-Ionen+ ist größer als das OH–.
Basierend auf dieser Analyse ist es RICHTIG zu sagen, dass:
a) Nur die Aussagen I und II sind richtig.
b) nur die Aussagen I und III sind richtig.
c) nur die Aussagen II und III sind richtig.
d) Alle drei Aussagen sind richtig.
Richtige Alternative: b) nur die Aussagen I und III sind richtig.
ICH. RICHTIG Zitrone enthält Zitronensäure, die in Lösung H-Ionen freisetzt+ und so ist das System sauer.
II. FALSCH. Der pH-Wert liegt unter 7, was für ein saures System charakteristisch ist: Je näher der pH-Wert der Lösung an 0 liegt, desto saurer ist sie.
III. RICHTIG Der saure pH-Wert ist auf die hohe Konzentration an H-Ionen zurückzuführen+ in Lösung, da pH = - log [H+].
Für weitere Fragen mit kommentierter Auflösung, überprüfen Sie bitte:Übungen zu pH und pOH.