DAS osmotischer Druck es ist eine kolligative Eigenschaft, die dem Druck entspricht, der auf ein System ausgeübt werden muss, um ein spontanes Auftreten von Osmose zu verhindern.
Osmose ist der Übergang von Wasser von einem weniger konzentrierten (hypotonischen) zu einem stärker konzentrierten (hypertonischen) Medium durch eine semipermeable Membran, bis ein Gleichgewicht erreicht ist.
Um zu verhindern, dass die Osmose auf natürliche Weise beginnt und auftritt, ist es notwendig, externen Druck auf die konzentriertere Lösung auszuüben, um den Durchgang des Lösungsmittels in das konzentriertere Medium zu verhindern. Das ist der osmotische Druck.
Je konzentrierter die Lösung, desto höher sollte der osmotische Druck sein. Daher ist der osmotische Druck proportional zur Konzentration des gelösten Stoffes.
Wie berechnet man den osmotischen Druck?
Jede Lösung hat einen anderen osmotischen Druckwert. Der osmotische Druck lässt sich nach folgender Formel berechnen:
= M. EIN. T. ich
Wo haben wir die folgenden Variablen:
π = osmotischer Druck;
M = Konzentration in mol/L;
R = universelle Gaskonstante, deren Wert 0,082 atm entspricht. L. mol-1. K-1 oder 62,3 mm Hg L. mol-1. K-1;
T = Temperatur auf der absoluten Skala (Kelvin);
i = Van’t Hoff-Faktor, der das Verhältnis zwischen der Gesamtzahl der endgültigen und anfänglichen Partikel in ionischen Lösungen umfasst.
Übung gelöst
1. (Puccamp-SP) Gelegentlich wird die 0,30 M Glukoselösung in einer intravenösen Injektion verwendet, da sie einen osmotischen Druck hat, der dem des Blutes nahe kommt. Wie hoch ist der osmotische Druck in Atmosphären dieser Lösung bei 37 °C?
a) 1,00.
b) 1,50.
c) 1,76.
d) 7.63.
e) 9.83.
In Anbetracht der von der Frage bereitgestellten Daten haben wir:
M = 0,30 mol/l;
R = 0,082 atm. L. mol-1. K-1
T = 37° + 273 = 310 K
Diese Werte müssen Sie nun auf die Formel zur Berechnung des osmotischen Drucks anwenden:
= M. EIN. T. ich
π = 0,30. 0,082. 310
= 7,63 atm (Alternative)
Klassifizierung von Lösungen
Die Lösungen lassen sich nach dem osmotischen Druck in drei Typen einteilen:
- hypertonische Lösung: Hat einen höheren osmotischen Druck und eine höhere Konzentration an gelösten Stoffen.
- isotonische Lösung: Wenn die Lösungen den gleichen osmotischen Druck haben.
- Hypotonische Lösung: Hat einen niedrigeren osmotischen Druck und die Konzentration der gelösten Stoffe.

Die Bedeutung des osmotischen Drucks für Lebewesen
Kochsalzlösung ist eine Substanz, die nach den Prinzipien des osmotischen Drucks hergestellt wird. Es sollte mit einem osmotischen Druck angewendet werden, der dem im Körper vorkommt, dies verhindert die Rote Zellen keine Hämolyse erleiden oder schrumpfen.
Der osmotische Druck des Blutes beträgt ungefähr 7,8 atm. Für das korrekte Funktionieren des Organismus müssen die roten Blutkörperchen daher den gleichen osmotischen Druck aufweisen, um den normalen Wasserfluss in und aus den Zellen zu gewährleisten.
Bei Dehydration ist beispielsweise die Verwendung von Kochsalzlösung angezeigt, die im Verhältnis zu Blutzellen und anderen Körperflüssigkeiten isotonisch sein muss.
Kochsalzlösung hat die Funktion, das osmotische Gleichgewicht im Organismus wiederherzustellen. Das liegt daran, dass das Blut während der Dehydration konzentrierter wird als das Innere der Zellen, wodurch sie welken.
Osmose und Umkehrosmose
Wie wir gesehen haben, ist die Osmose es ist der Prozess, bei dem Wasser von der hypotonischen in die hypertonische Umgebung durch eine semipermeable Membran geleitet wird, bis das Gleichgewicht zwischen den Konzentrationen erreicht ist.
Inzwischen ist die Umkehrosmose Es ist ein Prozess der Trennung von Substanzen durch eine Membran, die den gelösten Stoff zurückhält. Das Lösungsmittel fließt vom konzentrierteren zum weniger konzentrierten Medium und wird vom gelösten Stoff durch eine Membran isoliert, die seinen Durchgang ermöglicht.
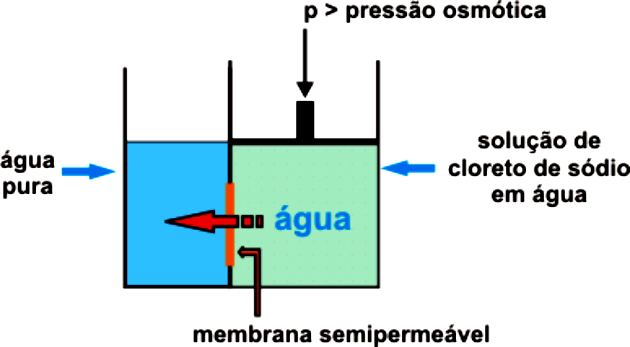
Dies geschieht nur aufgrund des ausgeübten Drucks, wodurch die semipermeable Membran nur den Durchgang von Wasser ermöglicht und den gelösten Stoff zurückhält. Dieser Druck muss größer sein als der natürliche osmotische Druck.
Wenn beispielsweise der aufgebrachte osmotische Druck größer als notwendig ist, tritt Umkehrosmose auf. Somit wird der Fluss vom Medium mit der höchsten Konzentration zum Medium mit der niedrigsten Konzentration übergehen.
