Das können wir festhalten Immer wenn wir die Konzentration eines oder aller an einer chemischen Reaktion beteiligten Reaktanten erhöhen, erhöht sich die Entwicklungsgeschwindigkeit, dh die Reaktionsgeschwindigkeit.
Das Gegenteil ist auch der Fall. Aktuell wird beispielsweise empfohlen, anstelle von normalem Alkohol Alkohol-Gel zu verwenden, da die Gefahr einer Verbrennung geringer ist und somit Unfälle vermieden werden. Gewöhnlicher flüssiger Alkohol ist eigentlich eine Mischung aus Alkohol und Wasser, wobei Gelalkohol eine geringere Alkoholmenge enthält. Daher läuft die Reaktion im Fall von Alkohol langsamer ab, wenn die Konzentration eines der Verbrennungsreaktanten verringert wird. Andererseits ist die Verbrennungsreaktion umso schneller, je reiner der Alkohol ist.

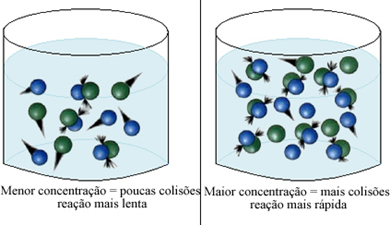
Wie im Text angegeben Bedingungen für das Auftreten chemischer Reaktionen, ist eine der Bedingungen für eine Reaktion die effektive Kollision zwischen den Teilchen. So, die Erhöhung der Konzentration der Reagenzien macht es möglich, eine größere Menge an Partikeln oder Molekülen in demselben Raum einzuschließen. Dies erhöht die Anzahl der Kollisionen zwischen ihnen und erhöht auch die Wahrscheinlichkeit, dass effektive Kollisionen auftreten, die zum Auftreten der Reaktion führen. Das Ergebnis ist, dass die Reaktion schneller abläuft.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Um dies zu sehen, denken Sie an das folgende Beispiel: Wenn wir eine brennende Glut haben und diese Verbrennung schneller ablaufen soll, blasen oder fächern wir die Glut an? Warum funktioniert das?
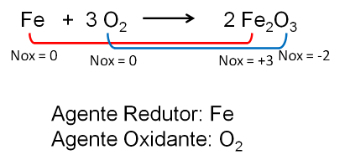
Nun, einer der Reaktanten bei dieser Verbrennungsreaktion ist Sauerstoff in der Luft. Beim Schütteln entfernt der Luftstrom die bei der Verbrennung entstehende Asche und erleichtert so den Kontakt des Sauerstoffs mit der Glut. Auf diese Weise erhöhen wir den Kontakt zwischen den Reaktanten und beschleunigen die Verbrennungsreaktion.
Kurz gesagt haben wir:

Wenn Sie mit Gasen arbeiten, können Sie die Konzentration der Reaktanten erhöhen: den Druck senken. Dabei verringern wir das Volumen und folglich steigen die Reagenzkonzentrationen.

Von Jennifer Fogaça
Abschluss in Chemie
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
FOGAÇA, Jennifer Rocha Vargas. "Konzentration der Reagenzien und Reaktionsgeschwindigkeit"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm. Zugriff am 27. Juni 2021.