Beim organische Eliminierungsreaktionen sind solche, bei denen Atome oder Atomgruppen eines Moleküls aus diesem entfernt oder eliminiert werden, Schaffung einer neuen organischen Verbindung, zusätzlich zu einer anorganischen Verbindung, die von dem Teil gebildet wird, der gelöscht.
Eine Art von Eliminierungsreaktion ist die Austrocknung, bei dem das verlorene Molekül Wasser ist. Die Dehydratisierung von Alkoholen (Verbindungen, bei denen die OH-Gruppe offen an einen gesättigten Kohlenstoff gebunden ist) kann auf zwei Arten erfolgen: intramolekular und intermolekular.
"Intra" bedeutet "innen", also Die intramolekulare Dehydratisierung von Alkoholen tritt auf, wenn ein Wassermolekül aus dem „inneren“ des Alkoholmoleküls selbst austritt. In diesem Fall ist das gebildete organische Produkt ein Alken.
Diese Reaktion findet nur in Gegenwart eines als Trockenmittel wirkenden Katalysators statt, meist ist es konzentrierte Schwefelsäure (H2NUR4) und die Temperatur sollte etwa 170 °C betragen.
Beispiel:
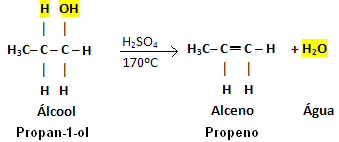
Beachten Sie, dass die OH-Gruppe übrig blieb und Wasserstoff den benachbarten Kohlenstoff verließ, wodurch Wasser entstand. Außerdem wurde die Doppelbindung gebildet, aus der das Alken entstand.
Die Möglichkeit, an Dehydration zu leiden, folgt der folgenden absteigenden Reihenfolge:
Tertiäre Alkohole > Sekundäre Alkohole > Primäre Alkohole
Aber was ist, wenn die OH-Gruppe in der Mitte der Kohlenstoffkette steht? Das Wasserstoffatom, aus dem benachbartes Kohlenstoffatom freigesetzt wird und das Wassermolekül bildet?
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Als nächstes kommt beispielsweise 2-Methylpentan-3-ol. Beachten Sie, dass ein benachbartes Kohlenstoffatom tertiär ist (rot hervorgehoben), während das andere sekundär ist (blau hervorgehoben):
H OH H
│ │ │
H3C─ Ç ─ Ç ─ Ç CH3
│ │ │
H H CH3
Der an das tertiäre Kohlenstoffatom gebundene Wasserstoff lässt sich leichter verlassen, da sein elektronegativer Charakter gleich δ. ist+1Je weniger negativ also der Charakter von Kohlenstoff ist, desto schwächer ist die Bindung zwischen ihnen und desto leichter ist es, ihre Bindung zu lösen.
In solchen Fällen werden alle möglichen Verbindungen gebildet, die Vorherrschaft wird jedoch in der Reihenfolge angegeben: Tertiäre Alkohole > Sekundäre Alkohole > Primäre Alkohole.
Also haben wir:
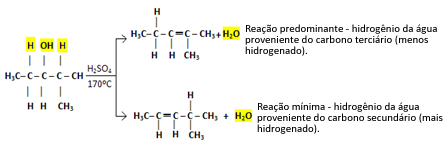
Diese Art der Reaktion gehorcht dem Saytzefs Regel, das sagt das Wasserstoff neigt eher dazu, weniger hydrierten Kohlenstoff zu hinterlassen. Diese Regel ist genau das Gegenteil von Markownikows Regel für Additionsreaktionen verwendet.
Um Ihr Wissen zu diesem Thema zu ergänzen, lesen Sie auch den Text "Intermolekulare Dehydratisierung von Alkoholen”.
Von Jennifer Fogaça
Abschluss in Chemie
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
FOGAÇA, Jennifer Rocha Vargas. "Intramolekulare Dehydratation von Alkoholen"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/desidratacao-intramolecular-dos-Alcoois.htm. Zugriff am 28. Juni 2021.