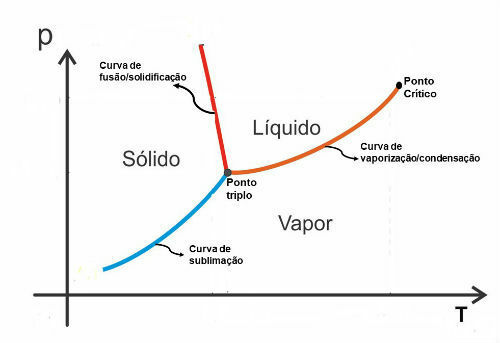
Es gibt einen Wissenschaftszweig, der die Geschwindigkeit chemischer Reaktionen und die Faktoren, die sie beeinflussen, untersucht, die chemische Kinetik. Chemische Reaktionen können als eine Reihe von Phänomenen definiert werden, bei denen zwei oder mehr Substanzen miteinander reagieren, wodurch unterschiedliche Verbindungen entstehen. Eine chemische Gleichung ist eine grafische Darstellung einer chemischen Reaktion, bei der Reaktanten im ersten Glied und Produkte im zweiten auftreten.
A + B  C + D
C + D
Reagenzien Produkte
Das Wissen und das Studium von Reaktionen sind nicht nur in industrieller Hinsicht sehr wichtig, sondern haben auch einen Bezug zu unserem täglichen Leben.
Die Reaktionsgeschwindigkeit gibt an, wie schnell Edukte verbraucht werden oder wie schnell Produkte gebildet werden. Das Abbrennen einer Kerze und die Bildung von Rost sind Beispiele für langsame Reaktionen. In Dynamit ist die Zersetzung von Nitroglycerin eine schnelle Reaktion.
Die Geschwindigkeiten chemischer Reaktionen werden durch empirische Gesetze bestimmt, die als Gesetze von bezeichnet werden Geschwindigkeit, abgeleitet aus dem Einfluss der Konzentration von Edukten und Produkten auf die Geschwindigkeit von Reaktion.
Chemische Reaktionen laufen mit unterschiedlichen Geschwindigkeiten ab und diese können verändert werden, denn zusätzlich zu Konzentration von Edukten und Produkten, Reaktionsgeschwindigkeiten auch von anderen Faktoren abhängig mögen:
Reagenzkonzentration: Je höher die Konzentration der Reaktanten, desto schneller verläuft die Reaktion. Damit eine Reaktion zwischen zwei oder mehreren Stoffen stattfinden kann, ist es notwendig, dass die Moleküle kollidieren, so dass die Bindungen brechen und sich neue bilden. Die Anzahl der Kollisionen hängt von den Konzentrationen von A und B ab. Siehe das Bild:
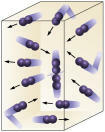
Moleküle kollidieren häufiger, wenn
wir erhöhen die Zahl der reagierenden Moleküle.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Es ist leicht zu erkennen, dass aufgrund einer höheren Konzentration die Kollisionen zwischen den Molekülen zunehmen werden.
Kontaktfläche: eine Vergrößerung der Kontaktfläche erhöht die Reaktionsgeschwindigkeit. Ein Beispiel ist, wenn wir eine zerkleinerte Sonrisal-Tablette auflösen und sie sich schneller auflöst als wenn es ein Ganzes wäre, geschieht dies, weil wir die Kontaktfläche vergrößern, die mit dem Wasser.
Druck: Wenn Sie den Druck eines gasförmigen Systems erhöhen, erhöht sich die Reaktionsgeschwindigkeit.
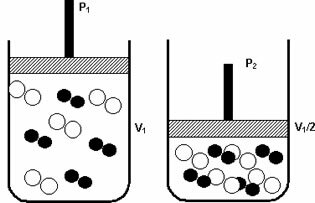
Eine Druckerhöhung von P1 auf P2 reduzierte das Volumen von V1 auf V1/2 und beschleunigte die Reaktion durch die Annäherung der Moleküle.
Die obige Abbildung zeigt beispielhaft, dass mit der Volumenabnahme im zweiten Behälter eine Zunahme des Druck verstärkt die Kollisionen der Moleküle und in der Folge eine Erhöhung der Geschwindigkeit der Reaktion.
Temperatur: wenn die Temperatur eines Systems erhöht wird, steigt auch die Reaktionsgeschwindigkeit. Eine Erhöhung der Temperatur bedeutet eine Erhöhung der kinetischen Energie von Molekülen. In unserem Alltag können wir diesen Faktor beim Kochen beobachten und erhöhen die Herdflamme, damit das Essen schneller den Gargrad erreicht.
Katalysatoren: Katalysatoren sind Stoffe, die den Mechanismus beschleunigen, ohne sich dauerhaft zu verändern, d. h. während der Reaktion nicht verbraucht werden. Katalysatoren ermöglichen der Reaktion einen alternativen Weg, der weniger Aktivierungsenergie erfordert, wodurch die Reaktion schneller abläuft. Es ist wichtig, sich daran zu erinnern, dass ein Katalysator die Reaktion beschleunigt, aber nicht die Ausbeute erhöht, dh er produziert die gleiche Produktmenge, aber in kürzerer Zeit.
Von Líria Alves
Abschluss in Chemie
Möchten Sie diesen Text in einer schulischen oder wissenschaftlichen Arbeit referenzieren? Aussehen:
SOUZA, Líria Alves de. "Chemische Kinetik"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/cinetica-quimica.htm. Zugriff am 27. Juni 2021.