Ö Phasendiagramm ist ein Diagramm, das es Ihnen ermöglicht zu definieren, in welchem physikalischen Zustand sich eine Substanz zu einem bestimmten Zeitpunkt befindet, wenn Sie ihre Temperatur und ihren Druck kennen.
Labormessungen werden verwendet, um das Phasendiagramm einer bestimmten Substanz zu erstellen.
Das Diagramm ist in drei Bereiche unterteilt, die den festen, flüssigen und dampfförmigen Zustand darstellen.
Die Punkte auf den Linien, die diese Bereiche begrenzen, geben die Temperatur- und Druckwerte an, die die Substanz in zwei Zuständen haben kann.
Ein Phasendiagramm hat die folgenden Elemente:
- Kurve von Verschmelzung: trennt die Bereiche, die festen und flüssigen Zuständen entsprechen.
- Kurve von Verdampfung: trennt die Bereiche, die der Flüssigkeits- und Dampfphase entsprechen.
- Kurve von Sublimation: trennt die Bereiche, die der festen und der Dampfphase entsprechen.
- dreifacher Punkt: Schnittpunkt der drei Kurven (Fusion, Vaporisation und Sublimation). Dieser Punkt gibt die Temperatur- und Druckwerte an, die der Stoff gleichzeitig in den drei Zuständen haben kann.
- Kritischer Punkt: gibt die höchste Temperatur an, bei der der Stoff verdampft. Ab diesem Zeitpunkt ist es nicht mehr möglich, zwischen flüssigen und dampfförmigen Zuständen zu unterscheiden. Bei Temperaturen oberhalb des kritischen Punktes wird der Stoff gasförmig.
In der folgenden Abbildung präsentieren wir eine Darstellung eines Phasendiagramms:

Lesen Sie mehr unter: Physikalische Zustandsänderungen.
Schmelzkurve
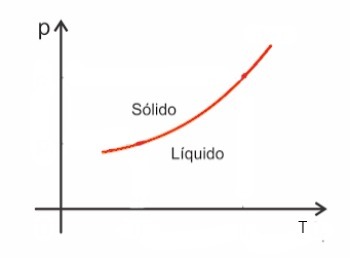
Stoffe nehmen im Allgemeinen an Volumen zu, wenn sie schmelzen, und nehmen im Gegenteil an Volumen ab, wenn sie erstarren. Als Folge führt eine Druckerhöhung zu einer Erhöhung des Schmelzpunktes (Schmelztemperatur).
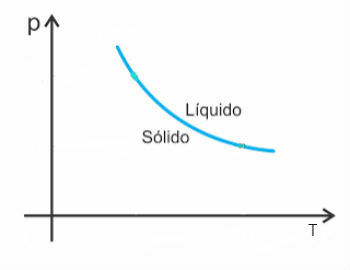
Es gibt jedoch einige Ausnahmen, darunter Wasser, das beim Schmelzen an Volumen abnimmt. In diesem Fall bewirkt eine Druckerhöhung eine Erniedrigung des Schmelzpunktes.
Somit sieht die Schmelzkurve dieser Stoffe wie folgt aus:
Beispiel
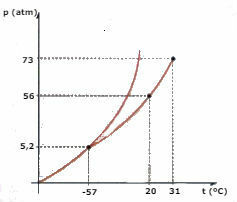
Betrachten Sie das CO-Phasendiagramm2 (Kohlendioxid) unten dargestellt und beantworten Sie die Fragen:
a) Welche Phase hat das CO2 , bei einer Temperatur von -60 °C und einem Druck von 50 atm?
b) Eine bestimmte Menge CO2 Flüssigkeit wird einem Druck von 56 atm ausgesetzt und in einem Behälter eingeschlossen. Wenn die Flüssigkeit erhitzt wird und der Druck konstant gehalten wird, bei welchem Temperaturwert findet die Verdampfung statt?
c) Welchen Temperatur- und Druckwert hat der Tripelpunkt von CO2?
d) Ein Stück Trockeneis (CO2) wird einem Druck von 2 atm ausgesetzt. Es wird erhitzt, wobei der Druck konstant gehalten wird. Zu einem bestimmten Zeitpunkt beginnt ein Phasenwechsel. Wie heißt diese Änderung?
Auflösung:
a) Betrachten wir das Diagramm, so schließen wir, dass das CO2 wird in der festen Phase sein.
b) Verdampfung tritt ein, wenn die Temperatur 20°C erreicht.
c) Der Tripelpunkt entspricht dem Schnittpunkt der drei Kurven, im Fall von CO2, bei einer Temperatur von -57 °C und einem Druck von 5,2 atm können die drei physikalischen Zustände nebeneinander existieren.
d) Sublimation wird auftreten
Um mehr zu erfahren, lesen Sie auch:
- Erstarrung
- Schmelz- und Siedepunkt
- Verdunstung
- Kondensation
Gelöste Übungen
1) Feind - 2000
Noch heute ist es üblich, Tonbehälter (Jerks oder unglasierte Keramiktöpfe) zu verwenden, um Wasser bei einer niedrigeren Temperatur als der Umgebungstemperatur aufzubewahren. Das ist weil:
a) Ton isoliert Wasser von der Umgebung und hält es immer auf einer niedrigeren Temperatur als seine eigene, als wäre es Styropor.
b) Ton hat aufgrund seiner chemischen Zusammensetzung die Fähigkeit, Wasser „einzufrieren“. Bei der Reaktion verliert Wasser Wärme.
c) der Ton ist porös und lässt Wasser durch. Ein Teil dieses Wassers verdunstet und entzieht dem Moringa und dem Rest des Wassers Wärme, die dann abgekühlt werden.
d) der Ton ist porös, sodass sich Wasser an der Außenseite des Krugs absetzen kann. Das Außenwasser hat immer eine höhere Temperatur als das Innenwasser.
e) Moringa ist eine Art natürlicher Kühlschrank, der hygroskopische Substanzen freisetzt, die die Wassertemperatur auf natürliche Weise senken.
Alternative c: Ton ist porös und lässt Wasser durch. Ein Teil dieses Wassers verdunstet und entzieht dem Moringa und dem Rest des Wassers Wärme, die dann abgekühlt werden.
2) Ita - 2013
Betrachten Sie das hypothetische Phasendiagramm, das in der folgenden Abbildung schematisch dargestellt ist:

Was bedeuten die Punkte A, B, C, D und E?
Punkt A: Sublimationspunkt
Punkt B: Tripelpunkt
C-Punkt: Schmelz-/Erstarrungspunkt
Punkt D: Verdampfungs-/Kondensationspunkt
Punkt E: kritischer Punkt
3) UECE - 2009
Betrachten Sie das unten gezeigte PT-Phasendiagramm. Daraus kann richtig geschlossen werden, dass eine Substanz, die den Sublimationsprozess durchlaufen hat, der Trajektorie folgt:

a) X oder Y
b) Y oder U
c) U oder V
d) T oder X
Alternative b: Y oder U