Vor der Einführung des Konzepts von Molmasse und MolzahlSchauen wir uns in diesem Zusammenhang einige wichtige Definitionen an:
→ molarer Term
Molar kommt vom Wort Molekül, aber was genau ist ein Molekül? Es ist die Menge von Atomen, die durch chemische Bindungen verbunden sind.
→ Molekulargewicht (MM)
Es ist möglich, die Masse eines Moleküls aus der Summe der Atommassen jedes Atoms zu berechnen, aus dem das jeweilige Molekül besteht. Das Ergebnis wird Molekulare Masse (MM) genannt.
Wie groß wäre die Molekülmasse von Schwefelwasserstoff (H2S) zum Beispiel?
Zuerst müssen Sie wissen, was das ist Atommasse jedes Atoms, das durch das Periodensystem von given gegeben ist Elemente.
Atommasse von Wasserstoff (H) = 1 amu. (Einheit pro Atommasse)
Atommasse von Schwefel (S) = 32,1 a.u.u.
Die Molekülmasse ist die Summe der Atommassen der Atome.
Hinweis: der Wasserstoff des H-Moleküls2S hat einen Koeffizienten von 2, also müssen Sie seine Masse mit 2 multiplizieren. Berechnung:
Molekulargewicht von H2S = 1 • 2 + 32,1 = 34,1 u
(H) + (S) = (H)2S)
Molmasse und Molzahl
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Sowohl die Molmasse als auch die Molzahl hängen mit der Avogadros Konstante (6,02 x 1023) durch das folgende Konzept:
''Die Anzahl der in 1 Mol enthaltenen Elementareinheiten entspricht der Avogadro-Konstante, deren Wert 6,02 x 10. beträgt23 mol-1.''
Daher ist die Molmasse die Masse von 6,02 x 1023 chemischen Einheiten und wird in g/mol ausgedrückt.
Mindmap - Mol
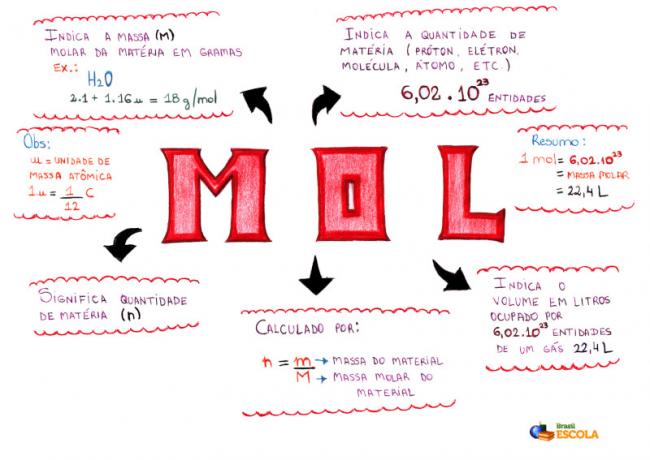
* Um die Mindmap herunterzuladen, Klicke hier!
Beispiel: H2so
Molekulargewicht = 34,1 u
Molmasse (M) = 34,1 g/mol
Dies bedeutet, dass wir bei 34,1 g/mol Schwefelwasserstoff 6,02 x 1023 Moleküle oder 1 Mol Schwefelwasserstoffmoleküle.
Fazit
Molekularmasse und Molmasse haben die gleichen Werte, der Unterschied ist die Maßeinheit. Die Molmasse hängt mit der Molzahl zusammen, die durch die Avogadro-Konstante gegeben ist.
* Mindmap von mir. Diogo Lopes
Von Líria Alves
Abschluss in Chemie
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
SOUZA, Líria Alves de. "Molmasse und Molzahl"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/massa-molar-numero-mol.htm. Zugriff am 27. Juni 2021.


