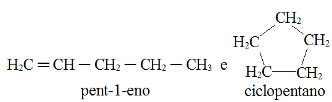Den officielle nomenklatur for etherne kan ifølge IUPAC udføres på to måder. Se hver enkelt:
1. vej:

Eksempler:
CH3 — O — CH2 — CH3→ mødteoxyetenO
CH3 — CH2 — O — CH2 —CH3→ etoxyetenO
CH3 — CH2 — O — CH2— CH2 —CH3→etoxyrekvisitenO
CH3 — O — CH2— CH═CH —CH3→ mødteoxymendaO
CH3 — CH2 — CH2 — O — CH2— CH2 — CH2 — CH2 — CH3→rekvisitoxypentenO
Hvis de er etere af lukkede kæder, nomenklaturen vil være anderledes:

Eksempler:
Stop ikke nu... Der er mere efter reklamen;)
2. vej:
De to grupper, der er knyttet til ilt, betragtes som substituenter, der er angivet i rækkefølgen af kompleksiteten med suffikset deres, det vil sige, det følger følgende regel:
æter + 1. gruppe + 2. gruppe + deres
Disse grupper skal vises og
Eksempler:
CH3— O —CH2 —CH3→ æter ethylderes og methylderes
CH3 —CH2—O —CH2 —CH3→æterdiethylderes
CH3 —CH2—O —CH2—CH2 —CH3→æterethylderes og propilederes
CH3 —CH2 —CH2—O —CH2—CH2 —CH2 —CH2 —CH3→æterpropilederes og pentylderes
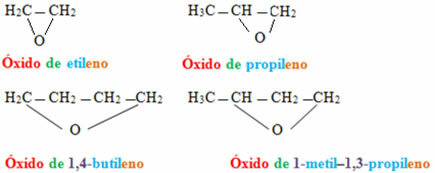
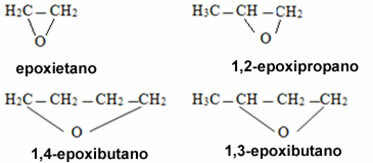
I tilfælde af cykliske forbindelser kaldes de epoxider:
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Eternes nomenklatur"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/nomenclatura-dos-Eteres.htm. Adgang til 27. juni 2021.
Basenomenklatur, vandig opløsning, ionisk dissociation, kation, anion, natriumhydroxid, aluminiumhydroxid, jernhydroxid, kobberhydroxid, jernhydroxid, calciumhydroxid.