DET kædeisomerisme er en type flad eller forfatningsmæssig isomerisme, dvs. hvor to eller flere forbindelser har den samme molekylformel (de samme kemiske grundstoffer og i samme mængde), men de adskiller sig efter formlen strukturel.
I tilfælde af kædeisomerisme (også kaldet kerneisomerisme eller skeletisomerisme) hører forbindelserne til den samme organiske funktion, men forskellen er i typen af kæde.
For eksempel kan vi have følgende tilfælde:
1 - Den ene isomer kan have en åben (acyklisk) kæde, mens den anden har en lukket (cyklisk) kæde;
2 - En isomer kan have kæden mættet (kun enkeltbindinger mellem carbonatomer), mens den anden isomer er umættet (har mindst en dobbeltbinding mellem carbonatomer);
3 - Den ene har den normale kæde, mens den anden har den forgrenede kæde;
4 - Den ene har den homogene kæde, og den anden har den heterogene kæde.
Hvis du har spørgsmål om disse typer kulstofkæder, skal du læse teksten Klassificering af kulstofkæder.
Se nu på nogle eksempler på kædeisomerisme:
1- Åben og lukket kæde:
De følgende isomerer har molekylformlen C5H10, men de adskiller sig ved, at den ene har en åben kæde og den anden har en lukket kæde:

Kædeisomerer (åben og lukket)
Derudover passer dette eksempel også ind i følgende type kædeisomerisme:
2- Mættet og umættet kæde:
I det forrige eksempel så vi, at kæden af pent-1-en er umættet, da den har en dobbeltbinding mellem to carbonatomer, mens cyclopentan er mættet, dvs. at den kun har enkeltbindinger.
Se et andet eksempel: Molekylær formel: C3H6:
CH2 ═ CH ─ CH3 og CH2
/ \
H2C CH2
propencyclopropan
Stop ikke nu... Der er mere efter reklamen;)
3- Normal og forgrenet kæde:
Denne type isomerisme kan forekomme i lukkede eller åbne kæder. For eksempel har cyclopentanen vist i den første vare ingen grene, men en anden af dens isomerer, methylcyclobutan, gør det. Se:

Kædeisomerer (normale og forgrenede)
Se nu på et eksempel på denne type isomerisme med åben kæde. Molekylformlen for de følgende isomerer er: C4H8O2:
H3C CH2 - CH2- COOH og CH3 ─ CH ─ COOH
│
CH3
Butansyre 2-methylpropansyre
4- Homogen og heterogen kæde:
En homogen kæde er en, der kun har kulstofatomer, mens en heterogen kæde er en, der har en heteroatom, det vil sige et atom med et eller andet kemisk element mellem carbonatomer, såsom ilt, nitrogen, svovl og fosfor.
Eksempel: C2H7N:
H3C ─ N - CH3 og H3C CH2 ─ NH2
│
H
dimethylamin-ethylamin
(heterogen) (homogen)
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Kædeisomerisme"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/isomeria-cadeia.htm. Adgang til 27. juni 2021.
Kemi
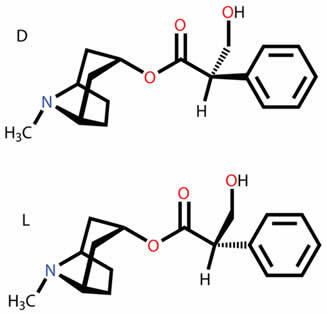
Ved hvad de forskellige typer plane og rumlige isomerer handler om, såsom funktion, position, kæde, tautomerisme, metamerisme, cis-trans geometrisk og optisk isomerisme.