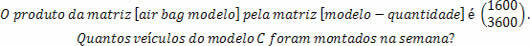En opløsning er en homogen blanding af to eller flere stoffer.. Som for eksempel en opløsning af salt (opløst stof) opløst i vand (opløsningsmiddel).

Især i kemiske laboratorier og industrier er denne proces meget vigtig, fordi kemikeren har brug for at fremstille løsninger med kendte koncentrationer. Desuden anvendes der eksperimentelle opløsninger med meget lave koncentrationer, så en prøve af den koncentrerede opløsning fortyndes til den ønskede koncentration.
På daglig basis adskillige gange, uden at vi er klar over det, udfører vi processen med at fortynde løsninger. For eksempel anbefaler emballagen til rengørings- og hygiejneprodukter, såsom desinfektionsmidler, at de fortyndes inden brug. Nogle producenter foreslår på produktetiketter, at det fortyndes med vand i en andel på 1 til 3, det vil sige, at for hver del af produktet skal der tilføjes 3 dele vand. Dette gøres, fordi produktet er meget koncentreret og stærkt og kan beskadige det sted, hvor det skal påføres, hvis det ikke fortyndes på den rigtige måde. På den anden side, hvis du fortynder det mere, end det burde, kan du miste penge, fordi produktet ikke opnår det ønskede resultat.

Et andet eksempel er når vi fremstiller juice. Etiketterne på mange saftkoncentrater indikerer, at et glas juice skal fortyndes eller blandes med 5 glas vand. Således bliver saften “svagere”, dvs. mindre koncentreret.
Forestil dig, at du har fortyndet en sådan juice i 3 liter vand. Hvis den oprindelige saftkoncentration var 40 g / L, betyder det, at den havde en masse på 40 g for hver liter opløsningsmiddel. Men da vi har 3 l, deles massen med 3, og koncentrationen vil derefter være ca. 13, 33 g / l eller 13 gram for hver liter opløsning. Imidlertid forbliver massen af 40 g opløst stof i hele opløsningen.
Beregningen af denne nye koncentration kan gøres som følger:
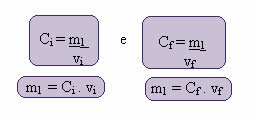
Hvor indekserne i og f repræsenterer henholdsvis de indledende og endelige værdier. Da værdien af m1 ikke er ændret, kan vi udligne ligningerne:
Çjeg. vjeg = Cf. vf
Udskift de værdier, vi har, ifølge det foregående eksempel, bemærk:
Indledende løsning:
Çjeg: 40 g / l
m1: 40 g
vjeg: 1L
Endelig løsning:
Çf: ?
m1: 40 g
vf: 3L
Çjeg. vjeg = Cf. vf
(40 g / l). (1 liter) = Cf. 3L
Çf = 40 g / l
3
Çf = 13,333 g / l
Den samme begrundelse gælder også for molkoncentrationen (M) og for masseprocenten af opløst stof eller titer (T):
Mjeg. vjeg = Mf. vf og Tjeg. vjeg = Tf. vf
Af Jennifer Fogaça
Uddannet i kemi
Brazil School Team
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/diluicao-solucoes.htm