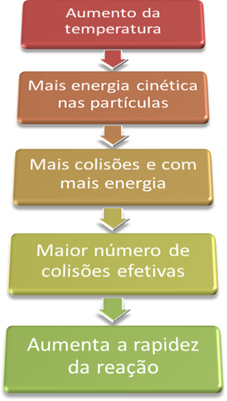
Jo højere temperaturen er, jo større er reaktionshastigheden.
Dette kan let ses i mange situationer i vores daglige liv som i følgende eksempler:
- Når vi ønsker at bremse nedbrydningsreaktionen på en mad, sænker vi temperaturen og lægger den i køleskabet.

- Hvis vi vil fremskynde madens tilberedningsreaktion, skal du bare lægge den i en gryde. tryk, som med stigende tryk også øger kogetemperaturen for det flydende vand, hvori mad er;

- Brande er generelt ødelæggende, fordi temperaturen i miljøet stiger, hvilket medfører en forøgelse af forbrændingsreaktionens hastighed;
- At bremse metaboliske kemiske processer og mindske chancerne for hjerneskade pga iltmangel, nogle operationer udføres ved at sænke patientens kropstemperatur og nå rundt 15 ° C;
- Hvis vi lægger en brusetablet i et glas varmt vand og en anden i et glas koldt vand, opløses den første meget hurtigere.
Men hvad forklarer temperaturens direkte proportionale indflydelse på reaktionshastigheden?
Stop ikke nu... Der er mere efter reklamen;)
Dette skyldes, som forklaret i teksten “
Betingelser for forekomst af kemiske reaktioner”For at en reaktion kan fortsætte, er det nødvendigt at tilfredsstille nogle betingelser, såsom at partiklerne de skal kollidere effektivt og med den krævede minimumsenergi, der kaldes aktiveringsenergi.Når vi således øger temperaturen i systemet, øger vi også omrøringen af de reagerende partikler og giver dem mere kinetisk energi. Med dette vil der forekomme flere kollisioner og med mere energi, hvilket øger mængden af partikler, der vil reagere og dermed øger reaktionshastigheden.
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Reaktioners temperatur og hastighed"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/temperatura-velocidade-das-reacoes.htm. Adgang til 27. juni 2021.