Hvad betyder det at sige, at en gas har gennemgået en gasformig transformation?
For at besvare det indledende spørgsmål er det vigtigt at huske, at tilstanden af gas eller gasformig tilstand bestemmes af tilstandsvariablerne: tryk, volumen og temperatur. Snart vil en gastransformation det er intet andet end enhver situation, hvor en bestemt mængde gas gennemgår variation i en af dens tre tilstandsvariabler. Hver gang en variabel gennemgår ændringer, vil en anden derfor få sin værdi ændret.
I det 17. århundrede gennemførte adskillige forskere eksperimenter for at opdage de særlige forhold ved gastransformationer. Blandt dem kan vi nævne: Torriceli, Robert Boyle, Mariotte, Guericke, blandt andre. I hans studier bestod proceduren i at ændre en af tilstandsvariablerne og observere de andres adfærd. Ved at gøre det observerede de, at for at bestemme forholdet mellem en variabel signifikant og en anden, det var nødvendigt at få den tredje til ikke at ændre sig, det vil sige at forblive konstant. Undersøgelserne blev således udført på tre forskellige måder, hver med sine særlige forhold, de er:
isoterm transformation, isobar transformation og isovolumetrisk transformation.Før vi beskriver de tre ovennævnte transformationer, skal vi huske, hvad Generel perfekt gaslov: I henhold til denne lov defineres en gasmasse oprindeligt af tilstandsvariabler (s1, V1 og T1), når den gennemgår en gasformig transformation, har den tilstandsvariablerne (s2, V2 og T2), der karakteriserer den endelige tilstand for gassen. Disse variabler følger følgende forhold:

Fra ovenstående ligning kan vi se, at tryk, volumen og temperatur varierer under gastransformationen.
Isoterm transformation ellerBoyle-Mariottes lov: er den transformation, hvor temperaturen T af gassen forbliver konstant og varierer dens tryk P og dens volumen V. Følgende liste er gyldig:

Isobarisk transformation ellerHomoseksuel-lov: er den transformation, hvor tryk P af gassen forbliver konstant og varierer dens volumen V og temperatur T. Følgende liste er gyldig:
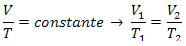
Isovolumetrisk transformation eller Charles Law: også kendt som isometrisk transformation, er den transformation, hvor volumen V af gassen forbliver konstant og varierer dens tryk P og temperatur T. Følgende liste er gyldig:

Af Nathan Augusto
Uddannet i fysik
Kilde: Brasilien skole - https://brasilescola.uol.com.br/fisica/as-transformacoes-gasosas.htm


