På nitriler, også kaldet cyanider, er en klasse af organiske forbindelser, hvori deres funktionelle gruppe (__C≡N) det opnås ved at erstatte brint i hydrogencyanidgassen (HCN - deraf navnet cyanid) med noget organisk radikal. Selve cyanidgassen betragtes som en nitril.
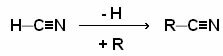
Nomenklatur:
Nomenklaturen for nitriler kan udføres på to måder:
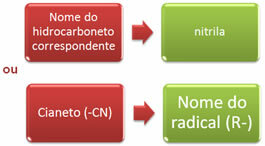
Eksempler:

Anvendelser, applikationer og indkøb:
Nitriler vises i forskellige dele af naturen, se nogle af disse apparationer:
* Pesticidekstraktion: Ethanonitrile, bedre kendt som acetonitril, er et opløsningsmiddel, der i vid udstrækning anvendes i organisk kemi til at ekstrahere pesticider fra prøver af planter, frø og sojaderivater. Dette gør det muligt at identificere, hvilke pesticider der blev brugt;
* Dyreforsvarssystem: polydesmiden er et blindt nedbrydeligt dyr, der lever i resterne af grøntsager, frugt og kød. Det beskytter sig selv ved at producere hydrocyansyre, som afværger sine fjender. Hydrocyansyre er hydrogencyanidgas i et vandigt medium, der frigiver H-ioner+ og CN-. Denne sidste ion er ekstremt giftig og kan dræbe;
* I frø og grøntsager: frø af frugter såsom ferskner, druer, kirsebær og æbler indeholder i små mængder en nitril kaldet amygdalin, hvis struktur er vist nedenfor. Derudover er denne forbindelse også til stede i blade og rødder af vild kassava. Derfor, når du fodrer denne grøntsag til kvæg, er det nødvendigt at hugge dem godt og lade dem tørre i solen, så HCN fordamper. Og når man laver mad til mennesker, er det nødvendigt at lave mad i lang tid;

*Fremstilling af syntetiske stoffer: acetonitril eller vinylcyanid er den nitril, der er mest brugt til denne type produktion;
* Metallurgi og galvanisering (galvaplastik): cyanidløsninger anvendes i vid udstrækning i industrier til disse formål;
* Forgiftninger: mange spion- eller politifilm viser, at kapsler indeholdende natrium- eller kaliumcyanid reagerer med saltsyre i maven og får personen til at dø af forgiftning. Et reelt tilfælde af dette var den russiske munk Rasputin, der i 1916 led et forsøg på forgiftning af cyanid, der blev blandet i en budding. Han døde ikke, fordi glucose og saccharose kombineres med cyanid for at generere cyanhydrin, som næsten ikke har toksicitet.
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/nitrilas-ou-cianetos.htm