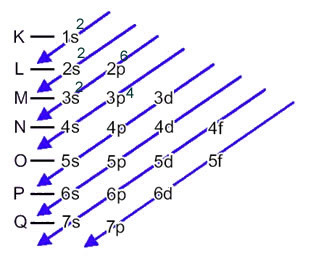
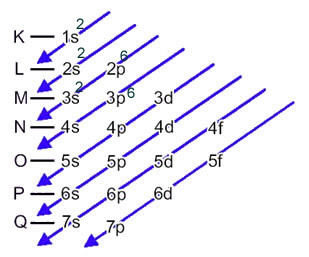
Elektronická distribuce elektronů atomu v neutrálním nebo základním stavu se běžně provádí s Paulingův diagram, je uvedeno níže:
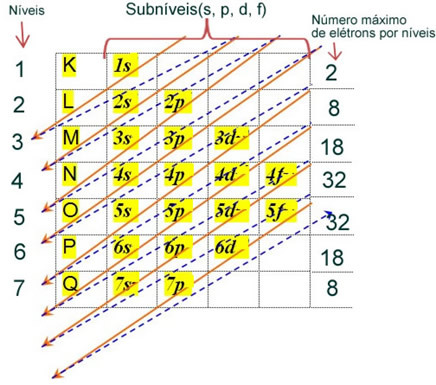
Podrobná pravidla této distribuce naleznete v následujících dvou textech na našem webu: “Elektronická distribuce elektronů" a "Pravidla elektronické distribuce”.
Elektronická distribuce iontů funguje zpočátku stejným způsobem jako u atomů v neutrálním stavu; s jediným rozdílem. Jelikož je iont atom, který získal nebo ztratil elektrony, musíme to vzít v úvahu a udělat následující:

Důležitým postřehem je: změna se provádí na nejvzdálenější podúrovni a není nejenergetičtější.
pokud je iont a kation, musíme odstraňte elektrony že prohrál. Podívejme se na příklad:
Atom železa (atomové číslo = 26) má následující elektronickou distribuci na nižších úrovních v energetickém pořadí: 1 s2 2 s2 2 s6 3 s2 3p6 4 s2 3d6. Pokud jde o elektronické vrstvy, máme: K =2; L = 8; M = 14; N = 2.
Tato distribuce je uvedena v Paulingově diagramu níže:
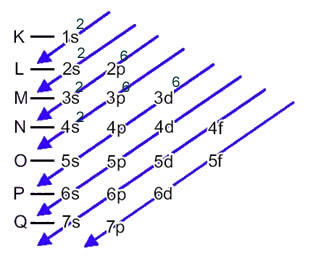
Když atom železa ztratí 2 elektrony, přemění se na Fe kation.
2+. Při vaší elektronické distribuci tedy musíme vyjměte 2 elektrony z poslední skořápky(N) a ne nejenergetičtější podúrovň, Jak je ukázáno níže: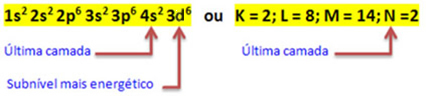
Tedy elektronická distribuce Fe kationtu2+ darováno:
1 s2 2 s2 2 s6 3 s2 3p6 3d6 nebo K = 2; L = 8; M = 14
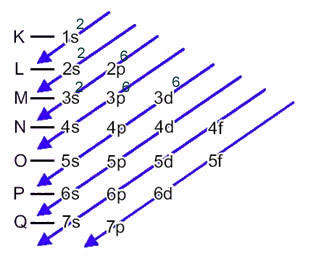
Nyní, pokud musíme provést elektronickou distribuci a anion, musíme přidejte elektrony, které přijal.Podívejte se, jak se to děje v následujícím příkladu:
Sirný anion (16s2-) se tvoří z atomu síry (16S) ziskem 2 elektronů, jak je naznačeno nábojem 2-. Jeho základní elektronická distribuce je dána:
1 s2 2 s2 2 s6 3 s2 3p4 nebo K = 2; L = 8; M = 6
V tomto případě je poslední úroveň nižší než úroveň nižší, 3p. Přidáme tedy dva elektrony aniontu síry:
1 s2 2 s2 2 s6 3 s2 3p6 nebo K = 2; L = 8; M = 8
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm

