Pokud by bylo možné velmi jasně vizualizovat strukturu kovu, viděli bychom to jako na obrázku výše. Atomová struktura kovů je krystalická, která se skládá z kovových kationtů obklopených elektrony.
Krystalické mřížky přítomné v kovech lze reprezentovat následovně: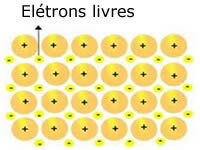
Zastoupení kovového sodíku (Na)
Krystalické mřížky kovů jsou tvořeny skupinou pevných kationtů.
Každý kation Na + je obklopen elektrony, ale ty jsou delokalizovány, to znamená, že nejsou přitahovány k žádnému jádru.
Protože mezi zápornými náboji (elektron) a kladným jádrem (kation) není přitažlivost, volné elektrony nakonec obsadí celou krystalickou mřížku kovu. Svoboda, kterou se elektrony musí pohybovat, způsobí, že vytvoří elektronický mrak.
Schopnost kovů vést elektřinu je vysvětlena přítomností tohoto mraku. Elektrický proud je výsledkem kontaktu volných elektronů s jinými kovy.
Ve složení jakéhokoli atomu, včetně kovů, jako je sodík (Na), zlato Au, měď (Cu), existuje valenční vrstva. Elektrony se volně pohybují touto vrstvou a udržují elektromagnetickou přitažlivost pro kationty. Tato strukturní vlastnost umožňuje tvorbu kovových molekul a následně i samotných kovů.
Líria Alves
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/como-se-forma-ligacao-metalica.htm