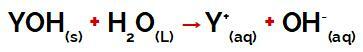Ó vinylchlorid je to a uhlovodík toxické chlorované a karcinogenní působení. Je to bezbarvý plyn při pokojové teplotě, je vysoce hořlavý a citlivý na teplo.
Je to monomer používaný při výrobě polyvinylchloridu, látky známé jako PVC. Ó PVC je tepelně odolný termoplast (na rozdíl od jeho monomeru), který má četné aplikace v každodenního života, jako je potahování elektrických vodičů, konstrukce potrubí a různých typů obal.
Přečtěte si také:Azbest — přírodní vlákno s širokým průmyslovým využitím, ale extrémně toxické pro člověka
Shrnutí o vinylchloridu
Vinylchlorid je chlorovaný uhlovodík se vzorcem H2C=CHCl.
Je to a plyn bezbarvý, sladce vonící a vysoce hořlavý.
Vinylchlorid je nestabilní vůči teplo, procházející rozkladem.
Hlavní použití vinylchloridu je při výrobě polyvinylchloridu (PVC).
PVC je termoplast s mnoha aplikacemi, jako je potrubí, díly, nátěry, obaly atd.
Vinylchlorid je toxický a má karcinogenní účinek.
vlastnosti vinylchloridu
molekulární vzorec: CH2CHCl (C2H3Cl).
Molekulová hmotnost: 62,498 g/mol.
fyzický stav: plyn (bezbarvý a se silným zápachem).
Hustota: 0,91 g/ml.
Rozpustnost ve vodě: velmi málo rozpustný (0,6 g ve 100 ml vody, 20 °C).
teplota tání: -154 °C.
Teplota varu: -13 °C.
Co je vinylchlorid?
Vinylchlorid je chlorovaný uhlovodík se vzorcem H2C=CHCl. Při pokojové teplotě se vyskytuje s a Bezbarvý a vysoce hořlavý plyn.
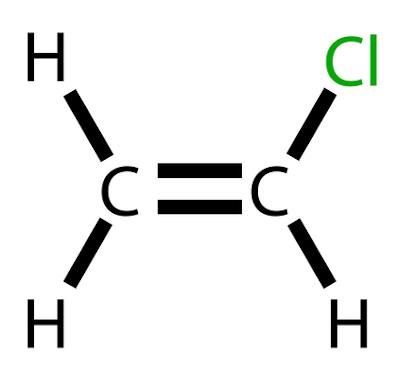
Vinylchlorid, také nazývaný chlorethen nebo vinylchloridový monomer, je a chemický produkt velkého významu v průmyslse speciálním uplatněním při výrobě polymer polyvinylchlorid, lépe známý jako PVC. Tato sloučenina zaujímá seznam 20 odvozených produktů ropa většího průmyslového a ekonomického významu.
Přečtěte si také:Benzopyren — karcinogenní uhlovodík nalezený v cigaretovém kouři a grilovaném mase
Vlastnosti vinylchloridu
Vinylchlorid je a Bezbarvý plyn s mírným, sladkým zápachem. Má tu vlastnost, že je vysoce hořlavý.
Při vystavení zdrojům tepla, může podléhat rozkladu a uvolňovat toxické výpary v oxid uhličitý, kysličník uhelnatý, chlorovodík a fosgen. Protože se jedná o organickou sloučeninu, její rozpustnost ve vodě je extrémně nízká, na druhou stranu je rozpustný v látkách jako např. ethanol, benzen a tetrachlormethan.
V přítomnosti vlhkosti se vinylchlorid stává korozivním a může napadnout žehlička a ocel. Má schopnost polymerovat při vystavení teplu v atmosférickém vzduchu prostřednictvím exotermické reakce. Tato vlastnost odvozuje mnoho z jeho průmyslových aplikací.
Vinylchlorid vyžaduje pozornost, protože je toxický a karcinogenní.
K čemu se používá vinylchlorid?
Vinylchlorid je monomer používaný k výrobě polymeru PVC (polyvinylchlorid) a další chlorovaná rozpouštědla.
PVC je termoplast používaný při výrobě obalů, obuvi, elektrických spojů a kabelů, dýmky, okna, hadičky a sáčky na odběr krve, oděvy a mnoho dalších položky.

Ó PVC vzniká polymerací vinylchloridu. V tomto chemickém procesu se velké množství molekul vinylchloridu k sobě přidává a vytváří velkou chemickou strukturu.
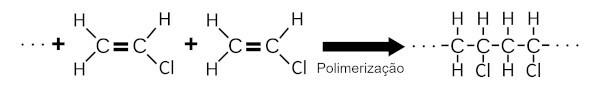
Ó PVC je retardér hoření a z tohoto důvodu je široce používán při potahování drátů, elektrických kabelů a nátěrů pro domácnosti.
Ačkoli vinylchlorid je chemická sloučenina, která vyžaduje pozornost kvůli své toxicitě a tepelná nestabilita, jeho PVC polymer je velmi stabilní vůči zdrojům tepla, je netoxický a lze jej skladovat bezpečně.
Do roku 1974 se vinylchlorid používal v aerosolech. V minulosti se dokonce používal jako inhalační anestetikum. S vědomím toxicity této sloučeniny byly tyto aplikace ukončeny.
Získání vinylchloridu
Syntéza vinylchloridu používaná v průmyslovém měřítku je iniciované sloučeninou ethylenem nebo ethenem (CH2=CH2) a může probíhat dvěma způsoby.
V prvním z nich se ethylen převádí na 1,2-dichlorethan reakcí s plynným chlorem. Poté se zahříváním 1,2-dichlorethanu v přítomnosti katalyzátoru získá vinylchlorid jako hlavní produkt a kyselina chlorovodíková jako sekundární produkt.
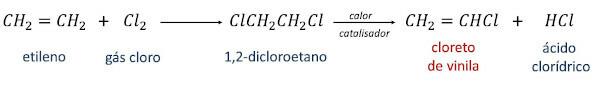
Ve druhé reakční cestě, známé jako oxychlorace, probíhá reakce mezi ethylenem, kyselinou chlorovodíkovou a kyslík ze samotné atmosféry, za přítomnosti tepla a katalyzátoru, generující vinylchlorid a vodu jako produkty.

Obvykle je výrobní centrum vinylchloridu postaveno tak, aby vyhovovalo oběma výrobním procesům. tak, že kyselina chlorovodíková generovaná v prvním způsobu působí jako činidlo pro provádění druhého způsobu trasa.
Preventivní opatření s vinylchloridem
Vinylchlorid je toxická sloučenina. Jelikož se jedná o plyn, Hlavní formou kontaminace je inhalace., proto musí být manipulace s ním vždy prováděna s použitím vhodného vybavení, jako jsou plynové masky.
Expozice této látce ovlivňuje nervový systém periferní a centrální, což způsobuje poškození játra. A Nepřetržitá expozice může spustit Raynaudův fenomén, což je soubor příznaků, které zahrnují bolesti kloubů a svalů a kožní změny, které mohou progredovat až do úplné ztráty elasticity kůže, dokonce orgány vnitřní orgány a krevní cévy.
Mezi další účinky patří euforie, dezorientace, potrat a vrozené vady. Zaznamenává se i poranění oční tkáně.
Příznaky závisí na úrovni expozice látce, od závratí, nevolnosti, poruch zraku, bolesti hlavy a ataxie při akutní expozici (od 1000 do 8000 ppm vinylchloridu ve vzduchu), narkotický účinek, srdeční arytmie a fatální respirační selhání v případech expozice hladinám nad 12 000 ppm.
Vinylchlorid a rakovina
Ó vinylchlorid je karcinogenní látka, spojené s vysokým rizikem rozvoje rakoviny jater, což může přispívat k výskytu rakovina mozku a plic, stejně jako rakovina lymfatického systému.
Přečtěte si také:Dusičnan amonný – sloučenina používaná v zemědělství, která může způsobit výbuchy
Výskyt vinylchloridu
vinylchlorid vzniká spontánně v prostředí rozkladem některých sloučenin obsahujících chlórpůsobením mikroorganismů. Proto může být považován za kontaminant vzduchu a vody, zejména v blízkých oblastech skládky.
Nejvyšší výskyt vinylchloridu je však syntetickými cestami souvisejícími s chemickým průmyslem, jak již bylo uvedeno výše.
Historie vinylchloridu
Vinylchlorid byl objeven v roce 1835 německým chemikem Justusem von Liebigem, při reakci dichlorethanu s hydroxidem draselným v alkoholovém prostředí.
Později, v roce 1872, chemik Eugen Baumann poprvé pozoroval polymeraci vinylchloridu, pocházejícího z PVC, poté, co náhodně opustil nádobu s látkou vystavenou Slunci.
V roce 1926 objevil americký vynálezce Waldo Semon chemické přísady, které zajišťovaly větší pružnost a tvárnost PVC, čímž se rozšířily možnosti použití této látky. Kolem roku 1950 se PVC začalo používat v průmyslovém měřítku. V současné době je PVC jedním z nejpoužívanějších termoplastů na světě.
Autor: Ana Luiza Lorenzen Lima
Učitel chemie
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/cloreto-de-vinila.htm