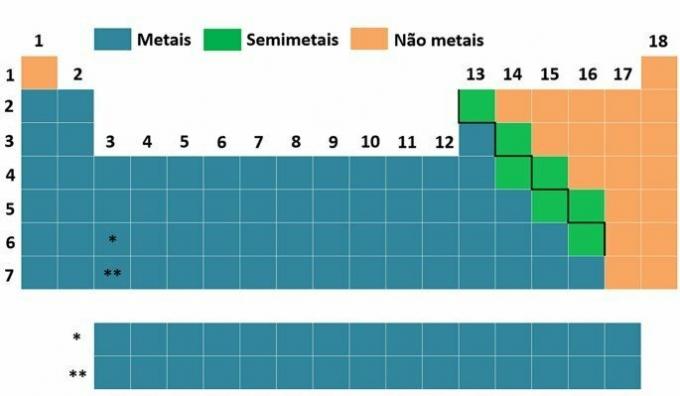
Ó titan je chemický prvek se symbolem Ti a atomovým číslem, tedy počtem protonů rovným 22. Tento kov se nachází ve skupině 4 a 4 periodické tabulky.
Atomová hmotnost prvku je 47,867 u, a protože má 22 elektronů v elektronech atomu, jeho elektronová distribuce je 1 s2 2s2 2p6 3s2 3p6 4s2 3d2.
Titan má žádoucí vlastnosti pro četné aplikace, protože je pevný jako ocel a mnohem lehčí.
Protože se jedná o tažný, žáruvzdorný, korozi odolný kov, vykazuje mechanickou odolnost, tepelná stabilita a nízká reaktivita, přidává se do kovových slitin tak, že mají vysok výkon. Díky své biokompatibilitě a netoxicitě je také užitečný pro výrobu kostních protéz.
Hlavní vlastnosti titanu jsou:
- Teplota tání: 1668 °C
- Bod varu: 3287 °C
- Hustota: 4,5 g/cm3
- Barva: stříbrná šedá
- Fyzikální stav při 20 °C: pevná látka
- Izotopy: Ti46, vy47, vy48, vy49 a vy50
Tento chemický prvek objevil Angličan William Gregor v roce 1791 a jeho název je odvozen z řečtiny titáni, později připsal Martin Heinrich Klaproth.
Titan je devátým nejrozšířenějším prvkem na planetě a nachází se v zemské kůře v rudách, jako je rutil (TiO
2) a ilmenit (FeTiO3). Proto je těžba hlavní metodou získávání tohoto kovu.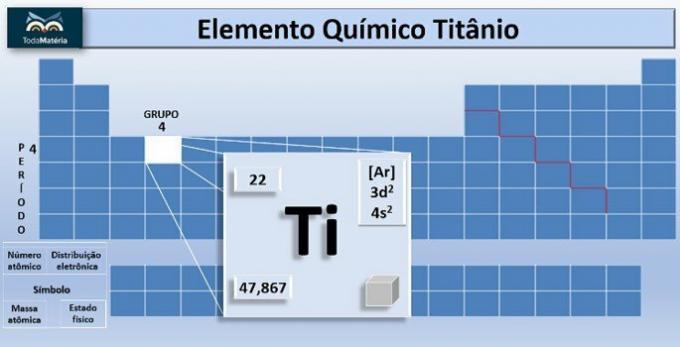
K čemu se používá titan?
Protože je při pokojové teplotě chemicky nereaktivní, snadno se formuje, má vysokou mechanickou odolnost a odolnost proti korozi, používá se titan jako strategický kov.
Letecký a letecký průmysl jsou hlavními uživateli titanu pro výrobu dílů, jako jsou součásti turbín a trupu. Dalšími aplikacemi jsou výroba zubních protéz, chirurgických implantátů a šperků.
V lékařství je titan velmi užitečný pro svou kompatibilitu s lidskými tkáněmi, lehkost a pevnost. Používá se k výrobě implantátů pro části těla, jako jsou mimo jiné fixační šrouby, náhrada kolenního kloubu, protéza humeru, protéza kyčle.
Oxid titaničitý (TiO2) je jednou z hlavních sloučenin tohoto prvku, která se používá jako bělicí činidlo. Vysoce kvalitní bílé inkousty jej obecně používají ke zlepšení vizuálního vzhledu barvy a lesku. Jiné produkty, jako jsou zubní pasty a opalovací krémy, také používají pigment. Existuje také aplikace jako potravinářské barvivo přidané do mléčných výrobků, sladkostí a nápojů.
V architektuře můžeme vidět použití titanu k pokrytí zakřivených konstrukcí v Guggenheimově muzeu v Bilbau v severním Španělsku.

V každodenním životě najdeme řadu produktů, které mají ve svém složení titan, jako jsou rámy jízdních kol, brýle a tenisové rakety.
V chemickém průmyslu se titan používá jako katalyzátor reakcí. Tímto způsobem je možné řídit rychlost reakce a zkrátit dobu tvorby produktu bez ovlivnění složení látek.
Automobilový průmysl studoval začlenění titanu do výroby automobilů za účelem snížení jejich hmotnosti a tím i snížení spotřeby paliva a zvýšení jejich zrychlení.
Získejte více znalostí s obsahem:
- Chemické prvky
- Periodická tabulka
- Co jsou kovy?
Bibliografické odkazy
ATKINS, P.W.; JONES, L. Principy chemie: zpochybňování moderního života a životního prostředí. 3.vyd. Porto Alegre: Bookman, 2006.
FELTRE, R. Základy chemie: sv. singl. 4. vyd. Sao Paulo: Moderna, 2005.
Lee, J. D. Ne tak stručná anorganická chemie. Překlad 5. vyd. Angličtina. Vydavatel Edgard Blucher Ltd. 1999.