THE izomerie je to jev pozorovaný, když jsou různé sloučeniny tvořeny stejným množstvím stejných typů atomů.
Proto můžeme najít chemické látky se stejným molekulárním vzorcem a různými strukturními vzorci nebo prostorovým uspořádáním.
Tento jev je široce pozorován v organické chemii, která studuje sloučeniny uhlíku. Protože každý atom tohoto prvku může vytvářet 4 chemické vazby, je možné pozorovat různé kombinace.
Vzhledem k tomu, že změna uspořádání atomů dává vzniknout novým látkám, mají v důsledku toho různé fyzikální a chemické vlastnosti.
Když řekneme, které sloučeniny jsou izomery znamená, že mají stejné části, protože slovo je kombinací dvou výrazů řeckého původu: isos, znamená „opravdu“ a pouhý, což jsou „části“.
Dvě hlavní skupiny izomerie jsou rovina a prostor (stereoizomerie).
THE plochá izomerie lze jej zobrazit pomocí plochého strukturního vzorce sloučenin a má pět tříd: poloha, funkce, řetězec, kompenzace a tautomerie.
THE vesmírná izomerie pozoruje se orientací sloučenin a dělí se na geometrické (cis-trans) a optické.
Pojem izomerie zavedl v roce 1830 švédský vědec Jacob Berzelius.
Příklady izomerů
THE řetězová izomerie nastává, když se stejná sada atomů spojí a vytvoří struktury stejné funkční skupiny, ale s různými řetězci.
Příklad: molekulární vzorec C4H10 uhlovodíku může být přímý nebo rozvětvený.

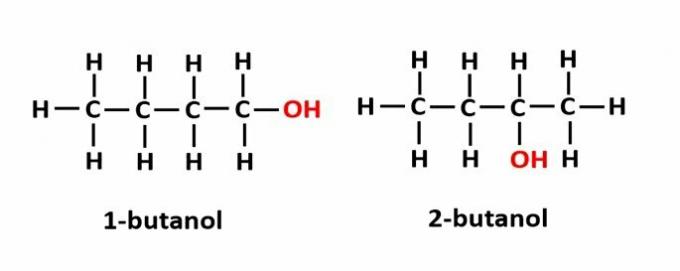
THE polohová izomerie nastává, když jsou sloučeniny tvořeny stejnými funkčními skupinami, ale jsou na různých pozicích v řetězci.
Příklad: Molekulární vzorec C4H9OH odpovídá dvěma druhům alkoholu.
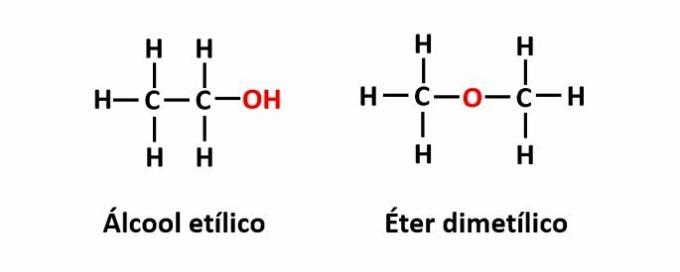
THE funkční izomerie nastává, když stejný molekulový vzorec odpovídá dvěma sloučeninám s různými funkčními skupinami.
Příklad: Molekulární vzorec C2H6O odpovídá dvěma izomerům, které mají alkoholovou (-OH) a etherovou (-O-) funkci.
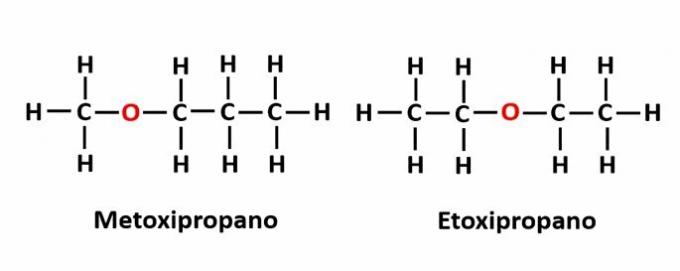
THE kompenzační izomerie nastává, když je v řetězci heteroatom a zaujímá různé pozice. Toto je zvláštní případ poziční izomerie.
Příklad: Molekulární vzorec C4H10Symbol označuje přítomnost atomu kyslíku v řetězci, ale jeho poloha se může měnit a tvořit různé sloučeniny.
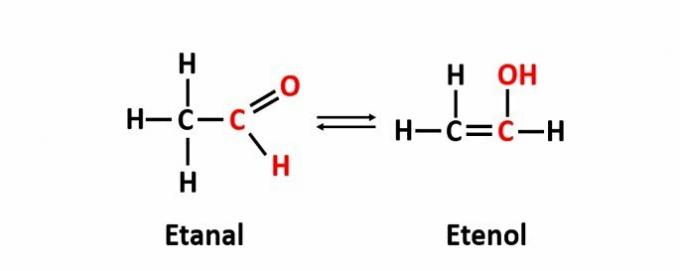
THE dynamická izomerie, také nazývaná tautomerie, nastává, když jsou dvě sloučeniny s různými funkcemi ve stejném roztoku v dynamické rovnováze. Toto je zvláštní případ izomerie funkce.
Příklad: Molekulární vzorec C2H4O odpovídá sloučeninám s aldehydovou a enolovou funkcí.
Dozvědět se víc o plochá izomerie.
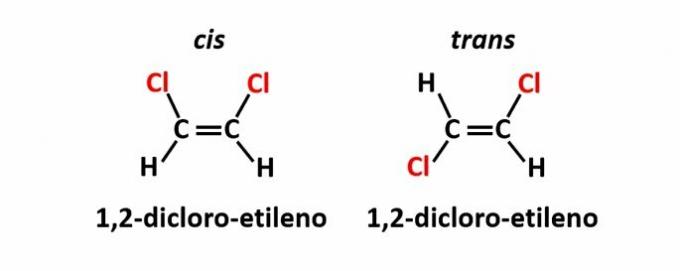
THE geometrická izomerie, nazývaný také izomerie cis-trans, nastává, když přítomnost dvojné vazby nebo cyklické struktury způsobí, že stejné ligandy jsou na stejné straně roviny (cís) nebo na opačných stranách (trans).
Příklad: atomy chloru ve sloučeninách molekulového vzorce C2H2Cl2 mohou mít dvě prostorové struktury.
THE optická izomerie nastává, když při vychylování polarizovaného světla vyzařovaného na konstrukci se sloučeninám podaří vychýlit paprsek svítící doleva, jde-li o levotočivý (l) izomer, nebo doprava, jde-li o pravotočivý izomer (d).
Příklad: Tento typ izomerie se vyskytuje u kyseliny mléčné. Všimněte si níže, že spektrální obrazy izomerů se nepřekrývají, proto se nazývají enantiomery.
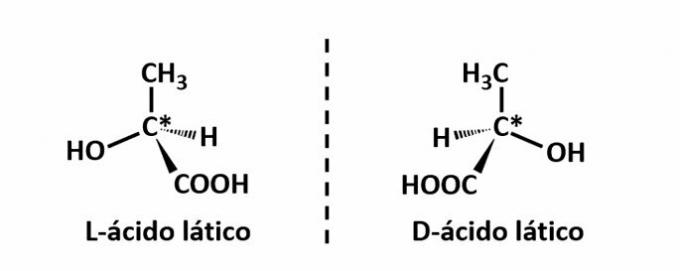
Symbol C* označuje přítomnost chirálního uhlíku v této struktuře, tj. atom uhlíku se 4 různými linkery.
Zjistěte více o izomerii s obsahem:
- Typy izomerie
- vesmírný izomer
- geometrický izomer
- optický izomer
- Cvičení o rovinné izomerii



