Dusičnany jsou anorganické sloučeniny, které obsahují anion NO3-.
Dusík je rodina 15, má 5 elektronů ve valenčním obalu a potřebuje vytvořit tři kovalentní vazby (se sdílením elektronů) mít osm elektronů ve valenčním obalu a tím mít stabilní. Každý kyslík má však v posledním obalu 6 elektronů, a proto každý jeho atom potřebuje vytvořit dvě vazby, aby byl stabilní.
Takže v dusičnanovém aniontu je dusík centrálním prvkem, který vytváří dvojnou vazbu s jedním z kyslíků, který je stabilní, jednoduchá vazba s jedním z dalších dvou kyslíků a s druhým kovalentní vazba dativ. To znamená, že jeden z kyslíků není stabilní a potřebuje přijmout o 1 elektron více, což dává celkový náboj rovný -1. S dativním dusíkem vytvoří vazbu více, než by dokázal, darováním jednoho ze svých elektronů získá náboj rovný +1. Podívejte se níže na strukturu tohoto aniontu:
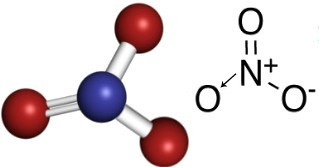
Tento anion může přijmout elektron a vytvořit elektricky neutrální sloučeninu, anorganickou sůl. Všechny tyto sloučeniny jsou rozpustné ve vodě.
Hlavní použití nitrátů je v lécích, jako jsou vazodilatátory při léčbě anginy pectoris (bolesti způsobené nízkým přísunem kyslíku průtokem krve do srdečního svalu) a erektilní dysfunkcí mužský. Používají se také v hnojivech a výbušninách, jak bude uvedeno později.
Dusičnany lze vyrobit neutralizační reakcí kyseliny dusičné (HNO).3) s nějakým základem. Viz příklad níže, kde vznikl dusičnan hořečnatý:
HNO3 + Mg(OH)2 → Mg (NO3)2+ H2Ó
Tři hlavní příklady tohoto typu sloučenin jsou dusičnan sodný (NaNO3), dusičnan draselný (KNO3) a dusičnan amonný (NH4NA3). Ve všech těchto případech jsou kationty (Na+,K+ a NH4+) poskytne 1 elektron dusičnanovému aniontu. Ale ve skutečnosti se tyto opačné náboje navzájem přitahují a tvoří dobře definované iontové shluky, což jsou krystalové mřížky. Dusičnany jsou tedy obvykle krystalické pevné látky, jak je uvedeno níže v případě dusičnanu sodného:
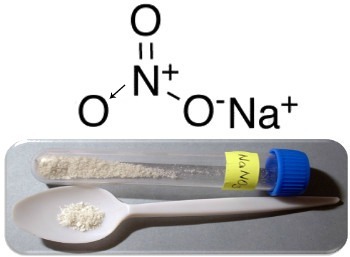
Tato sloučenina se používá při výrobě hnojiv, ale je známá především jako chilský ledek, neboť v chilských pouštích jsou jeho velká ložiska. Přeměňuje se na dusičnan draselný, který se používá k výrobě černého prachu používaného v různých zbraních a výbušninách.

Jak dusičnan sodný, tak dusičnan draselný se nazývají „ledek“ a jsou široce používány jako konzervanty barvy konzerv a uzeného masa a také v některých potravinách pro lepší pocit sytosti. Jeho konzumace však způsobuje vážné poškození zdraví, protože tyto dusičnany mohou být přeměněny bakteriemi z organismu na dusitany a později na nitrosaminy, které jsou karcinogenní, způsobují především rakovinu žaludek. Dusitany také přeměňují hemoglobiny v krvi, takže nejsou schopny přenášet kyslík.
Hlavními příčinami nadměrného příjmu dusičnanů je používání dusíkatých hnojiv při pěstování zeleniny.
Ledek je také nebezpečný, protože zvyšuje koncentraci sodíkových iontů v těle, což může způsobit srdeční problémy, jako je vysoký krevní tlak.
Ó dusičnan amonný používá se také jako hnojivo a výbušnina a byl dokonce použit s topným olejem při teroristickém útoku na budovy Světového obchodního centra 11. září 2001.

Při útoku na Světové obchodní centrum byl použit dusičnan amonný*
* Autorská práva k obrázku: Dan Howell a Shutterstock.com
Autor: Jennifer Fogaça
Vystudoval chemii
