Chemický izomerismus je jev pozorovaný, když dvě nebo více organických látek má stejný molekulární vzorec, ale odlišnou molekulární strukturu a vlastnosti.
Chemické látky s těmito vlastnostmi se nazývají izomery.
Termín je odvozen z řeckých slov iso = stejné a pouhé = části, tj. stejné části.
Existují různé typy izomerismu:
- plochý izomer: Sloučeniny jsou identifikovány plochými strukturními vzorci. Je rozdělen na izomerismus řetězce, izomerismus funkcí, izomerismus polohy, izomerismus kompenzace a izomerismus tautomerismu.
- vesmírný izomer: Molekulární struktura sloučenin má různé prostorové struktury. Je rozdělena na geometrický a optický izomerismus.
plochý izomer
Na plochá izomerie nebo konstituční izomerismus, molekulární struktura organických látek je plochá.
Sloučeniny, které vykazují tuto vlastnost, se nazývají ploché izomery.
izomer řetězce
K izomerismu řetězců dochází, když mají atomy uhlíku různé řetězce a stejnou chemickou funkci.
Příklady:
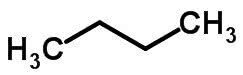
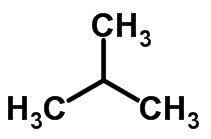
Funkční izomerismus
K izomerismu funkcí dochází, když dvě nebo více sloučenin mají různé chemické funkce a stejný molekulární vzorec.
Příklady: Tento případ je běžný mezi aldehydy a ketony.
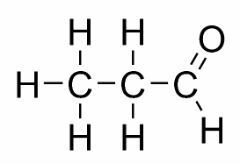
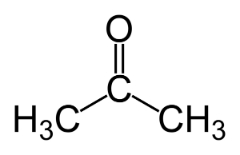
Poziční izomer
Poziční izomerismus nastává, když jsou sloučeniny rozlišeny různými polohami nenasycení, větvení nebo funkčních skupin v uhlíkovém řetězci. V tomto případě mají izomery stejnou chemickou funkci.
Příklady:

ofsetový izomer
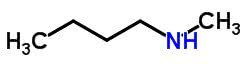
Kompenzační izomerismus nebo metamerismus se vyskytuje ve sloučeninách se stejnou chemickou funkcí, které se liší polohou heteroatomů.
Příklady:

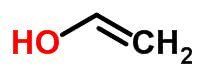
Tautomery
Tautomerismus nebo dynamický izomerismus lze považovat za specifický případ funkčního izomerismu. V tomto případě se jeden izomer může změnit na jiný změnou polohy prvku v řetězci.
Příklady:

vesmírný izomer
THE vesmírná izomerie, nazývaný také stereoizomerismus, nastává, když dvě sloučeniny mají stejný molekulární vzorec a různé strukturní vzorce.
V tomto typu izomerismu jsou atomy distribuovány stejným způsobem, ale zaujímají různé pozice ve vesmíru.
geometrický izomer
THE geometrický izomerismus nebo cis-trans se vyskytuje v nenasycených otevřených řetězcích a také v cyklických sloučeninách. K tomu musí být uhlíkové ligandy odlišné.

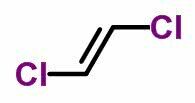
- Pokud jsou stejné ligandy na stejné straně, nomenklatura izomerů obdrží předponu cis.
- Když jsou stejné ligandy na opačných stranách, nomenklatura obdrží předponu trans.
IUPAC (International Union of Pure and Applied Chemistry) doporučuje, aby místo cis a trans byla jako předpona použita písmena Z a E.
Je to proto, že Z je první písmeno německého slova zusammen, což znamená „společně“. A je to první písmeno německého slova entegegen, což znamená „naproti“.
optický izomer
THE optická izomerie je demonstrována sloučeninami, které jsou opticky aktivní. Stává se to, když je látka způsobena úhlovou odchylkou v rovině polarizovaného světla.
- Když látka ohýbá optické světlo doprava, nazývá se to pravák.
- Když látka ohýbá optické světlo doleva, je látka vyvolána levotočivý.
Látka může také existovat ve dvou formách, které jsou opticky aktivní, dextogyra a levogyra. V tomto případě se to nazývá enantiomer.
Aby byla sloučenina uhlíku opticky aktivní, musí být chirální. To znamená, že jejich ligandy se nemohou překrývat, protože jsou asymetrické.
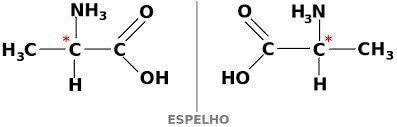
Na druhé straně, pokud má sloučenina dextrogyru a levotočivou formu ve stejných částech, říká se jim racemické směsi. Optická aktivita racemických směsí je neaktivní.
Přečtěte si také:
- Uhlík
- Organická chemie
- Molekulární vzorec
- strukturní vzorec
Cvičení
1. (Mackenzie 2012) Číselný sloupec B, který obsahuje organické sloučeniny a spojuje je se sloupcem A, podle typu izomerismu, který každá organická molekula představuje.
Sloupec A
1. ofsetový izomer
2. geometrický izomer
3. izomer řetězce
4. optický izomer
Sloupec B
() cyklopropan
() ethoxyethan
() bromchlor-fluormethan
() 1,2-dichlorethen
Správná posloupnost čísel ve sloupci B, shora dolů, je
a) 2 - 1 - 4 - 3.
b) 3 - 1 - 4 - 2.
c) 1 - 2 - 3 - 4.
d) 3 - 4 - 1 - 2.
e) 4 - 1 - 3 - 2.
Alternativa b) 3 - 1 - 4 - 2.
2. (Uerj) Izomerie je jev, který se vyznačuje skutečností, že stejný molekulární vzorec představuje různé struktury.
Vezmeme-li v úvahu plochý strukturní izomerismus pro molekulární vzorec C4H8, můžeme identifikovat izomery následujících typů:
a) řetěz a poloha
b) řetězec a funkce
c) funkce a kompenzace
d) poloha a kompenzace
Alternativa a) řetězec a pozice
3. (OSEC) Propanon a isopropenol jsou příkladem případu izomerismu:
a) metamerie
b) funkce
c) tautomery
d) cis-tran
e) řetěz
Alternativa c) tautomery
Podívejte se taky: Cvičení na plochém izomerismu

