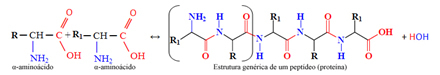
Jednoduché látky jsou složeny pouze z jednoho chemického prvku; pokud máte ve složení dva nebo více prvků, látky se skládají.
Studium reakcí chemického rozkladu bylo důležité při vývoji chemie, protože umožňovalo klasifikaci látek.
Vědci poznamenali, že ne všechny látky lze rozložit, a tak pomocí tohoto pozorování určili, zda jsou čisté látky jednoduché nebo složené.
U nich se složené látky rozdělily na nové látky, zatímco jednoduché látky nepodléhaly rozkladu.
Ačkoli tento koncept dnes již není přijat, výzkumy prováděné v této oblasti byly důležité pro rozvoj vědy.
jednoduché látky
Jednoduché látky tvoří jen chemický prvek, ale způsob atomy organizovat k jejich výrobě se může lišit takto:
- Existují atomy, které zůstávají izolované.
- Existují atomy, které se seskupují různými způsoby a mohou tvořit různé látky.
Příklad:
| izolovaný atom | více než jeden atom | |
|---|---|---|
| on | Ó2 | Ó3 |
| Hélium představující jak chemický prvek, tak molekulu hélia. | Spojení dvou atomů kyslíku tvoří molekulární kyslík a spojení tří atomů tvoří molekulu ozonu. |
Atomicita
Počet atomů v jednoduché látce představuje její atomicitu. Proto existuje následující klasifikace:
- Monatomické molekuly: tvořen pouze jedním atomem.
- Diatomické molekuly: tvořený dvěma atomy.
- triatomové molekuly: tvořený třemi atomy.
Příklady jednoduchých látek

složené látky
Sloučeniny se také nazývají chemické sloučeniny, které vznikají při chemických reakcích atomy nebo ionty různých prvků.
Příklad:
| Atomy | ionty |
|---|---|
| Dvě jednoduché látky (č2 a H2) reagují a tvoří sloučeninu (NH3). | Kation (Na+) a anion (Cl-) reagují a tvoří sloučeninu (NaCl). |
Stejně jako u jednoduchých látek lze chemické sloučeniny skládat z atomů v různých poměrech.
To se děje s vodou (H2O) a peroxid vodíku (H2Ó2). Oba jsou tvořeny pouze vodíkem a kyslíkem, ale počet atomů v látkách je odlišný, a proto tyto sloučeniny odlišují.
Dozvědět se více o: vodík a kyslík.
Příklady složených látek
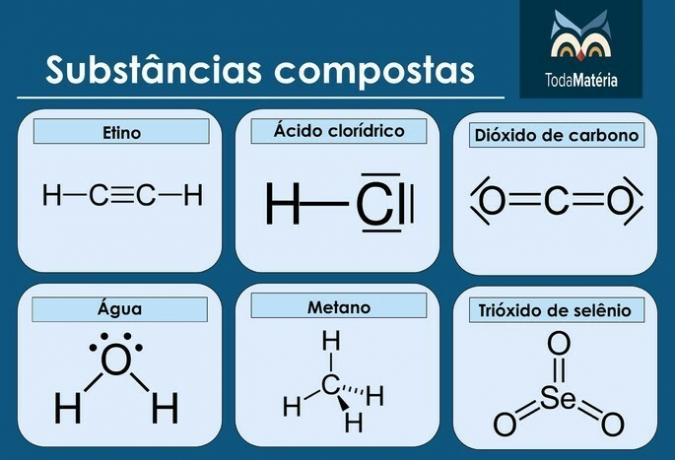
Cvičení s komentovanou zpětnou vazbou
1. (Cesgranrio) Určete alternativu, která v pořadí uvádí správné výrazy, které vyplňují mezery v následujícím prohlášení:
„Látka _____ je tvořena _____ a obsahuje pouze _____ stejné _____.“
a) kompozitní; molekuly; elementy; atom.
b) kompozitní; molekuly; atomy; živel.
c) chemie; elementy; molekuly; atom.
d) jednoduché; atomy; molekuly; živel.
Je to jednoduché; molekuly; atomy; živel.
Správná alternativa: e) jednoduchá; molekuly; atomy; živel.
a) NESPRÁVNÉ. Složená látka je molekula, pokud ve svém složení obsahuje atomy různých chemických prvků.
b) NESPRÁVNÉ. Složená látka je tvořena atomy různých chemických prvků a ne stejným prvkem.
c) NESPRÁVNÉ. Molekuly jsou skupiny atomů prvků spojených kovalentními vazbami.
d) NESPRÁVNÉ. Molekuly jsou tvořeny atomy chemických prvků.
e) SPRÁVNĚ. „Látka jednoduchý je tvořen molekuly, obsahující pouze atomy stejné živel.”
1) Vzduch je homogenní materiál složený z jednoduchých látek.
2) Z látek alkohol, zlato, diamant a aceton je pouze zlato jednoduchou látkou.
3) Měřením teplot tání a varu je možné rozlišovat mezi jednoduchými a složenými látkami.
4) Procesy separace materiálů se používají k získání jednoduchých látek z kompozitních látek.
1) NESPRÁVNÉ. Vzduch je směs plynů, ale ne všechny jsou jednoduché látky.
Jednoduché látky přítomné ve vzduchu jsou: dusík, kyslík a vzácné plyny. Existuje však také vodní pára a oxid uhličitý, což jsou složené látky.
2) NESPRÁVNÉ. Alkohol i aceton jsou složené látky klasifikované jako organické sloučeniny. Zlato a diamant jsou jednoduché látky.
Alkohol je chemická sloučenina, jejíž obecný vzorec je R-OH. Aceton je obchodní název propanonu, sloučeniny, která má vzorec CH3(CO) CH3.
Zlato představuje chemický prvek se symbolem Au a je kovem velké hodnoty, který se v přírodě nachází ve formě nuggetů. Diamant je krystal složený pouze z atomů uhlíku.
3) NESPRÁVNĚ. Teploty tání a teploty varu jsou fyzikální vlastnosti hmoty, které se používají k rozlišení materiálu od látky.
4) NESPRÁVNÉ. V separačním procesu lze získat jak jednoduché, tak složené látky.
Příklad:
Pyrolýzou vody vznikají dvě jednoduché látky: vodík a kyslík.
Fotolýzou peroxidu vodíku vznikne sloučenina a jednoduchá látka: voda a kyslík.
Podívejte se také: Organické funkce
3. (Mackenzie) Počet jednoduchých látek mezi látkami vzorce: O3, H2O, Na, P4, CH4, CO2 a Co je:
a) 2.
b) 3.
c) 4.
d) 5.
e) 7.
Správná alternativa: c) 4.
Celkem se ve výroku objevují čtyři jednoduché látky, zatímco ostatní jsou složeny.
Jednoduché látky:
- Ó3: Molekula ozonu tvořená atomy prvku kyslíku.
- Na: Izolovaný atom prvku sodíku.
- P4: Molekula fosforu složená ze čtyř atomů prvku.
- Co: Izolovaný atom kobaltového prvku.
Složené látky:
- H2O: Voda se skládá z atomů dvou prvků: vodíku a kyslíku.
- CH4: Metan je tvořen atomy dvou prvků: uhlíku a vodíku.
- CO2: Oxid uhličitý je tvořen atomy dvou prvků: uhlíku a kyslíku.
Podívejte se také: Chemické vazby
4. (UFPA) Vzhledem k reakci:
Mezi činidly a produkty jsou přítomny:
a) 2 jednoduché látky a 2 sloučeniny.
b) 1 jednoduchá látka a 3 sloučeniny.
c) 3 jednoduché látky a 1 sloučenina.
d) 4 jednoduché látky.
e) 4 složené látky.
Správná alternativa: a) 2 jednoduché látky a 2 sloučeniny.
jednoduché látky:
- C: Izolovaný atom prvku uhlík.
- H2: Molekula tvořená atomy prvku vodík.
složené látky:
- H2O: Voda se skládá z atomů dvou prvků: vodíku a kyslíku.
- CO: Oxid uhelnatý je tvořen atomy dvou prvků: uhlíku a kyslíku.
Podívejte se také: Směsi
5. (UFRGS) Žula se skládá ze čtyř minerálů: živce, magnetitu, slídy a křemene. Pokud lze jeden z těchto minerálů oddělit od ostatních, lze říci, že žula je:
a) prvek
b) jednoduchá látka
c) složená látka
d) iontová sloučenina
e) směs
Správná alternativa: e) směs.
a) NESPRÁVNÉ. Žula je tvořena chemickými sloučeninami zvanými oxidy. Oxidy mají různé chemické prvky, jako je křemík a hliník, kombinované s kyslíkem.
b) NESPRÁVNÉ. Jednoduchá látka se skládá z atomů pouze jednoho prvku. Žula je tvořena kombinací prvků v různých poměrech.
c) NESPRÁVNÉ. Složení žuly je proměnlivé a obsahuje několik složených látek. Nejběžnější jsou: SiO2Al2Ó3, K.2na2O, CaO, FeO a Fe2Ó3.
d) NESPRÁVNÉ. Iontové sloučeniny mají své atomy spojené iontovými vazbami. Oxidy, anorganická funkce přítomná v žule, jsou binární sloučeniny tvořené kovalentními vazbami, ve kterých jsou sdíleny elektrony.
e) SPRÁVNĚ. Žula je směs minerálů ve tvaru skály. Jejími složkami jsou:
- Živec: minerál složený z křemičitanu hlinitého, který obsahuje různé podíly vápníku, draslíku a sodíku. Jeho chemický vzorec je: (K, Na, Ca) (Si, Al)4Ó8.
- Magnetit: minerál tvořený oxidy železa II a železa III: Jeho chemický vzorec je: FeO.Fe2Ó3.
- Slída: minerál tvořený hydratovanými silikáty hliníku, draslíku, sodíku, železa, hořčíku a lithia. Příkladem slídy je: KAl2[Si3Ahoj10] (OH, F2)).
- Křemen: minerál tvořený oxidem křemičitým. Jeho chemický vzorec je: SiO2.
Mohlo by vás také zajímat: Předmět: co to je, složení a příklady.