Substituční (syntetické) reakce jsou reakce, které nastávají, když skupina daného činidla změní pozici se skupinou jiného činidla. Nejčastěji se vyskytují ve sloučeninách s vysokou stabilitou (s nasycenými řetězci). K těmto syntézám často dochází za účasti tepla nebo ultrafialového světla v reakčním médiu.
Vy alkany jsou to organické sloučeniny, které jsou náchylné podstoupit substituční reakce, protože mají pouze nasycené řetězce (pouze jednoduché vazby mezi atomy uhlíku). Jsou široce používány pro syntézy, které pocházejí z organických halogenidů, jako je methylchlorid (plyn používaný jako anestetikum).
Nejběžnější substituční reakce s alkany jsou:
halogenace;
nitrace;
sulfonace;
a) Halogenace
Jedná se o syntézu, při které molekula alkanu reaguje s molekulou halogenu (Cl2, br2, Já2 a F2). Použití I2 není to tak životaschopné, protože podporuje extrémně pomalou reakci. Již použití F2 nedoporučuje se to, protože jde o výbušnou reakci, která ničí organické látky.
Pro halogenaci alkanů s Br2 nebo Cl
2 přihodit se, je nutná přítomnost světla (λ) nebo silné zahřátí. Bez ohledu na použitý halogen bude konečným produktem této substituční reakce vždy a organický halogenid. Substituce poté proběhne mezi atomem vodíku alkanu na uhlíku a atomem halogenu, což povede k organickému halogenidu a halogenidu kyseliny (anorganické kyseliny). Viz příklad:
Pokud má alkan počet atomů uhlíku větší než dva, budeme mít nahrazení vodíku halogenem podle následujícího pořadí priority:
H v terciárním uhlíku> H v sekundárním uhlíku> H v primárním uhlíku
V následujícím příkladu vidíme, že H sekundárního uhlíku byl nahrazen atomem Br.
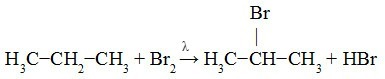
Pozorování: kdykoli má alkan více než dva uhlíky, vytvoří se více než jeden organický halogenid. Množství vytvořených halogenidů bude následovat pořadí priority. Podívejte se na několik příkladů:
Butanová bromace:
V rovnici níže pozorujeme tvorbu 2-brombutanu (ve větším množství, protože je to priorita v substituce v důsledku výměny prováděné na sekundárním uhlíku) a 1-brombutan (v menší míře) částka).
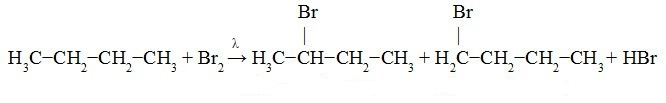
2-brombutan 1 -brombutan
Chlorace methylpropanu:

2-chlor-1-chlor-
2-methyl-2-methyl-
propan propan
Nepřestávejte... Po reklamě je toho víc;)
b) Nitrace
V této reakci kyselina dusičná (HNO3) reaguje s alkanem výměnou alkanového vodíku za nitroskupinu (NO2) kyseliny, což má za následek a nitrosloučenina a v molekule vody. Protože máme přítomnost kyseliny, není nutné používat katalyzátor.
Pozorování: stejná pravidla priority používaná pro výměnu vodíku při halogenaci se používají při nitraci.
Sledujte nitraci pentanu:
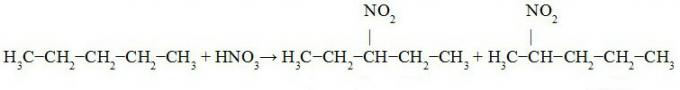
3-nitro-pentan 2-nitro-pentan

1-nitro-pentan
Ve výše uvedené rovnici jsme pozorovali tvorbu 3-nitro-pentanu (ve větším množství, protože je to priorita v nahrazení kvůli výměně být prováděno na terciárním uhlíku), 2-nitro-pentan (výměna vodíku na sekundárním uhlíku) a 1-nitro-pentan (v malém částka).
c) Sulfonace
V této reakci kyselina sírová (H2POUZE4) reaguje s alkanem výměnou alkanového vodíku za sulfonovou skupinu (SO3H) kyseliny, což má za následek a kyselina sulfonová a molekula vody. Protože máme přítomnost kyseliny, není nutné používat katalyzátor.
Pozorování: stejná pravidla priority používaná pro výměnu vodíku při halogenaci se používají také při sulfonaci.
Sledovat sulfonaci pentanu:

Kyselina penta-3-sulfonová Kyselina penta-2-sulfonová
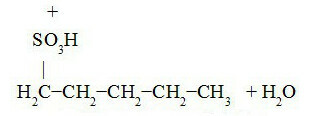
Kyselina penta-l-sulfonová
Podle mě. Diogo Lopes Dias
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
DNY, Diogo Lopes. "Náhradní reakce v alkanech"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-alcanos.htm. Zpřístupněno 28. června 2021.
Chemie

Alkany, uhlovodíky, metan, nasycené řetězce, alifatické, parafiny, paliva, benzín, minerální vosk, ropa, ropná břidlice, zemní plyn, petrochemický průmysl.
Alkánová nomenklatura, uhlovodíková funkce, uhlíkové valence, Mezinárodní unie Čistá a aplikovaná chemie, IUPAC, nasycené alifatické uhlovodíky, jednoduché vazby, sloučeniny Organické.
Chemie

Klikněte sem a dozvíte se více o substituční reakci, chemickém procesu, při kterém si použitá činidla (organická a anorganická) vyměňují jednu ze svých složek navzájem a vytvářejí nové látky. Mezi látky, které se nejčastěji používají jako činidla, patří alkany, benzen a organické halogenidy.