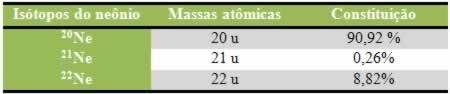
Vědec Friedrich Kohlrausch (1840-1910) jako první navrhl, aby čistá voda vedla elektřinu, i když v malém měřítku. Je to proto, že se voda chová amfoterně; to znamená, že při určitých příležitostech působí jako kyselina a daruje protony (H.+); a v jiných se chová jako základna a přijímá protony.
To znamená, že voda provádí svou vlastní ionizaci podle chemické rovnice uvedené níže:
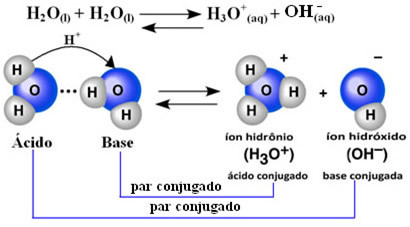
Tento proces se nazývá autoionizace vody a vyskytuje se ve velmi malém měřítku, to znamená, že voda je velmi slabý elektrolyt, s nízkými hodnotami stupně ionizace a ionizační konstanty v rovnováze (KC). To je přesně důvod, proč má voda tak nízkou vodivost.
Pro představu, při teplotě okolí 25 ° C je možné určit, že koncentrace hydroxidových a hydroniových iontů produkovaných při samoionizaci čisté vody jsou rovny 1. 10-7 mol. L-1. To znamená, že z miliardy molekul vody ionizují pouze dvě.
Konstanta iontové rovnováhy vody se nazývá Cdisociační konstanta vody,konstanta autoprotolýzynebo iontový produkt vody.Tuto konstantu představuje K.w, protože w odkazuje na slovo voda, což v angličtině znamená voda.
Nepřestávejte... Po reklamě je toho víc;)
Jeho výpočet se provádí stejným způsobem jako u ostatních rovnovážných konstant, přičemž je třeba pamatovat na to, jak je uvedeno v textu „Konstanty Balance Kc a Kp “, v tomto případě se ve výrazu objeví pouze produkty, protože voda v kapalném stavu má stejnou aktivitu až 1. Čisté kapalné nebo pevné látky se do disociačního konstantního výrazu nevkládají, protože se nemění. Jsou umístěny pouze vodné a plynné roztoky. Takže máme:
K.w = [H3Ó+]. [Ach-]
K.w = (1. 10-7). (1. 10-7)
K.w = 10-14
Stejně jako u ostatních rovnovážných konstant, OKw mění se pouze se změnou teploty. Jak se teplota vody zvyšuje, zvyšuje se také její ionizace, což znamená, že samoionizace vody je endotermický proces, tj. Absorbuje teplo.
To lze vidět na hodnotách iontového produktu vody (K.w) uvedené v tabulce níže při různých teplotách:
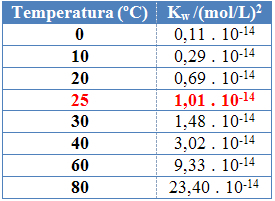
Iontový produkt vody bude mít vždy pevnou hodnotu při každé teplotě, ať už v čisté vodě nebo v roztoku. I když má roztok koncentrace iontů H3Ó+ a oh- různé, produkt mezi nimi zůstane konstantní.
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Ionic Water Product (Kw)“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/produto-ionico-Agua-kw.htm. Zpřístupněno 28. června 2021.