Jak je vysvětleno v textu Sytost řešení, vznikají chemické roztoky rozpuštěním a rozpuštěná látka na solventní. Každá rozpuštěná látka má a koeficient rozpustnosti specifické, což je maximální množství rozpuštěné látky v daném množství rozpouštědla v daném množství teplota.
Konstrukce grafu s křivkou rozpustnosti
Například koeficient rozpustnosti KNO3 je 31,2 g ve 100 g vody při 20 ° C. Pokud rozpustíme přesně toto množství dusičnanu draselného ve 100 g vody při 20 ° C, nasyceném roztoku. Jakékoli další množství této soli se vysráží (tvoří spodní část těla v nádobě).

Koeficient rozpustnosti se však mění s teplotou. Pokud tedy tento nasycený roztok zahřejeme spodní částí těla KNO3, sraženina se postupně rozpustí ve vodě. Níže uvidíte hodnoty koeficientů rozpustnosti KNO3 ve 100 g vody při různých teplotách:
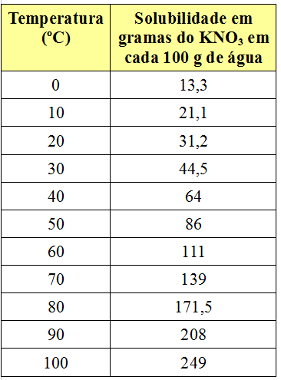
Všimněte si, že rozpustnost této soli ve vodě se zvyšuje se zvyšující se teplotou. U většiny látek je tomu tak také. Dáme-li tyto hodnoty do a grafický, budeme mít následující:
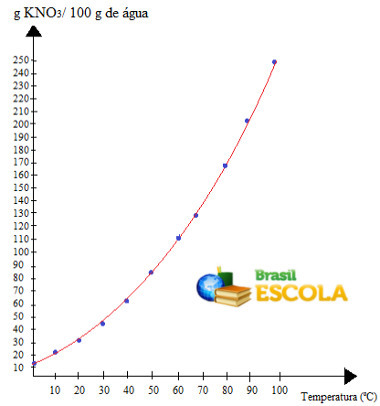
to je volání křivka rozpustnosti KNO3. Říkáme, že stoupá, protože roste s rostoucí teplotou.
Charakteristika křivek rozpustnosti rozpuštěných látek v grafu
Každá látka má své křivka rozpustnosti pro dané rozpouštědlo. Některé z těchto látek mají sníženou rozpustnost se zvyšující se teplotou, jako je tomu v případě CaCrO4, které mají křivka rozpustnosti dolů. To znamená, že pokud zahřejeme nasycený roztok této soli, část rozpuštěné soli se vysráží.
Pokud jde o jiné látky, zvýšení teploty příliš nenarušuje rozpustnost, jako je tomu u roztoku kuchyňské soli (NaCl). Při 20 ° C je koeficient rozpustnosti NaCl 36 g ve 100 g vody, ale pokud zvýšíme teplotu na 100 ° C, tato rozpustnost se zvýší pouze na 39,8 g, což je velmi malé zvýšení.
Nepřestávejte... Po reklamě je toho víc;)
Existují také látky, ve kterých se rozpustnost zvyšuje pouze do určitého bodu zvýšení teploty, protože poté se rozpustnost snižuje. To se děje například u hydratovaných látek, které při zahřátí dosáhnou doby, kdy dehydratují. Proto, jak se mění jeho složení, mění se také jeho variabilita s teplotou. Tento výskyt lze v grafu pozorovat inflexemi v křivce rozpustnosti.
Níže uvádíme a graf s křivkami rozpustnosti různých látek:
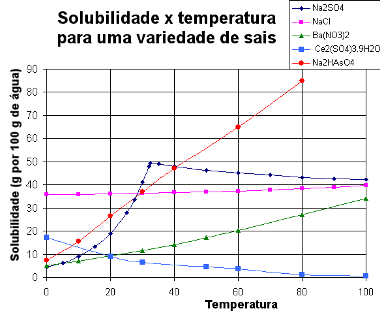
Křivky rozpustnosti různých solí
Prostřednictvím tohoto typu grafu můžeme porovnat rozpustnosti různých solí ve stejném rozpouštědle a za stejných teplot.
Klasifikace řešení pomocí grafu s křivkou rozpustnosti
Na křivky rozpustnosti také pomáhají určit sytost roztoků, to znamená, zda jsou nenasycené, nasycené, nasycené na pozadí nebo přesycené. Viz příklad:
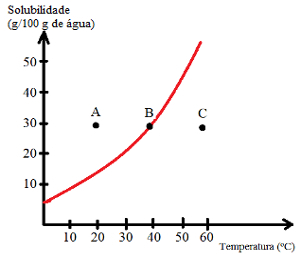
Podívejte se, jaké typy řešení jsou označeny body A, B a C:
Odpověď: Nasycená spodní částí těla. V bodě A se 30 g rozpuštěné látky rozpustí ve 100 g vody při 20 ° C. Křivka ukazuje, že v tomto bodě je koeficient rozpustnosti asi 15 g / 100 g vody. Jelikož je množství přítomné rozpuštěné látky větší, získá se nasycený roztok se spodním tělem.
B: Nasycené. Bod B je umístěn přesně na křivce rozpustnosti, což naznačuje, že roztok je nasycen, protože ve 100 g vody je při 40 ° C rozpuštěno 30 g rozpuštěné látky. To je tedy přesně koeficient rozpustnosti této rozpuštěné látky při této teplotě.
C: Nenasycené. Ve 100 g vody při 60 ° C je rozpuštěno 30 g rozpuštěné látky. Křivka ukazuje, že v tomto bodě je koeficient rozpustnosti větší než 50 g / 100 g vody. Jelikož je tedy množství rozpuštěné látky nižší než koeficient rozpustnosti, existuje nenasycený roztok.
Můžeme tedy dojít k závěru, že:
Body nad křivkou: nasycené roztoky s tělem pozadí;
Body na křivce: nasycené roztoky;
Body pod křivkou: nenasycené roztoky.
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. "Grafy křivek rozpustnosti"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/graficos-das-curvas-solubilidade.htm. Zpřístupněno 28. června 2021.
Chemie

Disociace a ionizace, italský vědec Volta, elektrický proud, švédský fyzikální chemik Svant August Arrhenius, teorie Arrhenius, kladné ionty, kationty, záporné ionty, anionty, hydroxid sodný, stolní sůl, polární molekuly, disociace iontový,