Vědět, že látky se mohou pohybovat z jednoho fyzického stavu do druhého, není nic nového. Ale jak přesně se to stalo? Jak se molekuly chovají, když tyto změny probíhají?
Pokud jde o kondenzaci (změna z plynu na kapalinu) a tuhnutí (kapalina na pevnou látku), podívejme se, jak k nim dochází na mikroskopické úrovni:
Kondenzace
Částice, když jsou v plynném stavu, ukládají velké množství energie, ale když procházejí chlazením, mají sníženou teplotu a v důsledku toho také svoji energii.
Jakmile je energie snížena, odpuzující síly mezi molekulami plynu mají tendenci klesat, a tudíž Tak je možná intermolekulární aproximace, která charakterizuje kapalný stav (molekuly plus sjednocený).
Nepřestávejte... Po reklamě je toho víc;)
Tuhnutí
Aglomerované částice, které tvoří kapalné skupenství, se mohou při chlazení ochladit. Jak teploty klesají, energie se odstraňuje. V tomto bodě se částice začnou srovnávat za vzniku pevné látky, což je proces známý jako tuhnutí.
Líria Alves
Vystudoval chemii
Tým brazilské školy
Vidět víc!Ovlivňuje intermolekulární síla teplotu a fyzikální stav molekuly?
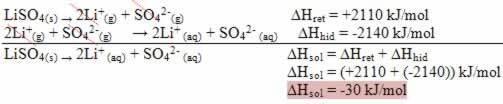
Entalpie ve změnách fyzického stavu.
Obecná chemie - Chemie - Brazilská škola
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Jak dochází ke změnám fyzického stavu v hmotě?“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/como-ocorrem-mudancas-estado-fisico-materia.htm. Zpřístupněno 27. června 2021.