أكسدة الطاقة في الألكاينات هو تفاعل عضوي يحدث عند إضافة ألكين (هيدروكربون له رابطة ثلاثية بين كربونين) إلى محلول حمضي مع كاشف باير (برمنجنات البوتاسيوم - KMnO4).
ملاحظة: رد فعل أكسدة الطاقة يمكن إجراؤها باستخدام ثنائي كرومات البوتاسيوم (K.2سجل تجاري2ا7) وليس فقط برمنجنات البوتاسيوم.
كلما رد فعل من يتم إجراء الأكسدة النشطة في الألكينات ، والمنتجات التي يمكن أن تنشأ الأحماض الكربوكسيليةوالماء (العنصر الوحيد الذي يظهر في أي منها) وثاني أكسيد الكربون (CO2).
كاشف باير في وسط حمضي
عندما يتم خلط كاشف Baeyer بالماء ، في وجود a حامض (مادة قادرة على إطلاق H أيونات+) ، هناك تشكيل اثنين أكاسيد (أكسيد البوتاسيوم وأكسيد المنغنيز II) والأكسجين الناشئ ([O]).

آليات أكسدة الطاقة في الألكينات
الآلية الأولى: كسر الرابطة الثلاثية.
في البداية ، تمت مهاجمة الرابطة الثلاثية بواسطة الأكسجين الناشئ الذي شكله كاشف باير. يتسبب هذا الهجوم في كسر الرابطة الثلاثية تمامًا.
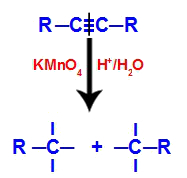
اضطراب الرابطة الثلاثية بهجوم الأكسجين الناشئ
عندما يتم كسر الرابطة الثلاثية ، يتم تقسيم الألكين إلى قسمين. على كل من ذرات الكربون التي كانت ترابطًا ثلاثيًا ، تظهر ثلاثة تكافؤات حرة.
الآلية الثانية: تفاعل مجموعات الهيدروكسيل
كل من التكافؤات الحرة على الكربون حيث تم احتلال الرابطة الثلاثية بواسطة مجموعات الهيدروكسيل (OH) ، مكونة بوليول (كحول مع عدة هيدروكسيل).
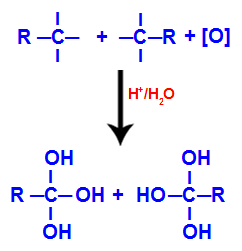
تشكيل البوليول مع مجموعات الهيدروكسيل بعد انقسام الرابطة الثلاثية
ملاحظة: إذا كان الكربون الذي كانت الرابطة الثلاثية فيه يحتوي على ذرة هيدروجين مرتبطة به ، فإن ذرة الهيدروجين ستتلقى أكسجينًا ناشئًا وتشكل أيضًا هيدروكسيلًا آخر.
الآلية الثالثة: تكوين جزيئات الماء
عندما يحتوي الكربون على مجموعتين أو أكثر من مجموعات OH ، يصبح هيكلًا غير مستقر للغاية بسبب وجوده للغاية الكهربية. وبالتالي ، بسبب عدم الاستقرار ، يخضع الجزيء للجفاف الذاتي ، أي يرتبط الهيدروكسيل بالهيدرونيوم (H+) من هيدروكسيل آخر ويشكل الماء.

تكوين جزيئات الماء من اثنين من الهيدروكسيل الموجود في البوليول المشكل
الآلية الرابعة: تشكيل المنتج
بعد تكوين جزيئات الماء ، يفقد الكربون الرابطة بسبب خروج أ يفقد الهيدروكسيل والأكسجين من الهيدروكسيل الآخر أيضًا الرابطة التي تم تكوينها باستخدام هيدروجين. لذلك ، بين هذا الكربون والأكسجين ، تظهر رابطة مزدوجة ، والتي تشكل الكربونيل (C = O) وتثبت كليهما.
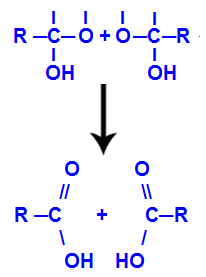
تم الحصول على تكوين الكربونيل في الهيكلين من الألكين
مثال على معادلة أكسدة الطاقة في الألكينات
مثال: أكسدة الطاقة لـ But-1-ino
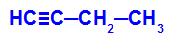
الصيغة الهيكلية لـ but-1-yne
عندما يتم وضع but-1-yne في وسط يحتوي على كاشف Bayer والماء والحمض ، تنكسر الرابطة. الثلاثي الموجود بين الكربون 1 و 2 ، بسبب هجوم الأكسجين الناشئ الموجود في الوسط ، كما في المعادلة أدناه:
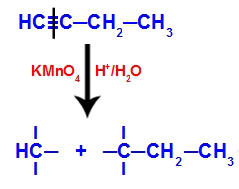
قطع الوصلات لكن -1-ين
بعد كسر الرابطة الثلاثية ، يتلقى الكربون 1 و 2 ثلاثة هيدروكسيل ، لكن الكربون 1 سيكون له واحد آخر لأن كان يحتوي على ذرة هيدروجين (التي ترتبط بالأكسجين الناشئ) ، مكونة اثنين من البوليولات (الجزء 1 و 2).

معادلة تمثل تكوين البوليولات
بعد فترة وجيزة ، نظرًا لأن البوليولات غير مستقرة ، يكون لدينا تكوين جزيئات الماء من الهيدروكسيل. في الجزء 1 ، يظهر جزيء ماء (لأن هناك ثلاثة هيدروكسيل) وفي الجزء 2 يظهر جزيئين (لأن هناك أربعة هيدروكسيل).
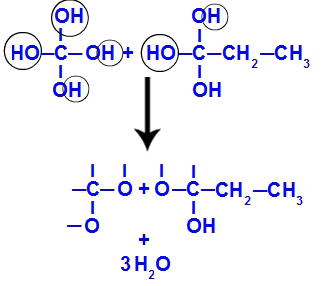
تكوين جزيئات الماء من شظايا ولكن -1-ين
أخيرًا ، لدينا تكوين الرابطة المزدوجة بين الكربون الذي فقد الهيدروكسيل والأكسجين الذي فقد الهيدروجين ، مما يؤدي إلى نشأة الكربونيل.

تشكيل كاربونيل في شظايا لكن -1-ين
مع المعادلة أعلاه ، يمكننا أن نرى أن 1-yne أدى إلى ظهور حمض الكربوكسيل وثاني أكسيد الكربون (CO2).
بي ديوغو لوبيز دياس
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcinos.htm

