التجارب طريقة عملية لتعلم واختبار معرفتك بالمفاهيم التي تمت دراستها في الكيمياء.
استفد من هذه التجارب الكيميائية ، والتي يمكن إجراؤها في المنزل (تحت إشراف الكبار) أو العمل عليها في الفصل مع المعلم ، لاستكمال دراستك.
التجربة الأولى - تفكيك الألوان
المفاهيم المتضمنة: الكروماتوغرافيا وفصل المخاليط
مواد
- أقلام (علامات مميزة) بألوان مختلفة
- كحول
- ورق ترشيح القهوة
- كوب (زجاج لتسهيل مراقبة التجربة)
كيف تصنع
- استخدم المقص وقطع شرائح من ورق الترشيح. لكل قلم مستخدم ، قم بعمل مستطيل.
- الآن ، على مسافة 2 سم تقريبًا من القاعدة ، ارسم دائرة بقلم اللون الذي اخترته وقم برسم كل الداخل.
- ألصِق حافة الورقة الأبعد عن قطعة الرخام المسحوبة على دعامة. لهذا ، يمكنك استخدام شريط وإرفاقه بقلم رصاص.
- أضف الكحول إلى الكوب ، وليس كثيرًا ، حيث يجب أن تلمس نهاية الورقة بالقرب من علامة القلم.
- ضع الورق في الكوب بحيث يكون رأسيًا. يجب أن يكون قلم الرصاص الذي يدعمها مستقرًا على الحواف.
- انتظر ما بين 10 و 15 دقيقة حتى يرتفع الكحول من خلال ورق الترشيح. بعد ذلك ، أزل الأوراق واتركها تجف.
نتيجة
عندما يمر الكحول عبر علامة القلم ، فإنه يتفاعل مع مكونات اللون ويدفعها عبر الورق. وبالتالي ، سيتم فصل الأصباغ المختلفة عن طريق ملامستها للكحول.
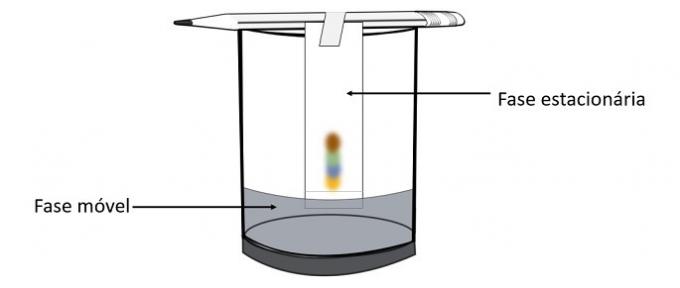
من خلال هذه التجربة ، من الممكن معرفة الألوان التي تم مزجها لإنشاء لون القلم.
تفسير
اللوني هو نوع من العمليات لفصل المخاليط. ورق الترشيح هو المرحلة الثابتة والكحول هو الطور المتحرك الذي يسحب مكونات الخليط أثناء مروره خلال المرحلة الثابتة. في هذه العملية ، كلما زاد التفاعل مع الكحول ، زادت سرعة تحرك الصبغة مع مرور المذيب.
سوف تتفاعل مكونات المادة مع الطور المتحرك ، بما أن لها خصائص مختلفة بطرق مختلفة ، والتي يمكن ملاحظتها من خلال أوقات السحب المختلفة في المرحلة الثابتة.
تعلم المزيد عن كروماتوغرافيا.
التجربة الثانية - حفظ الطعام
المفاهيم المتضمنة: المركبات العضوية والتفاعلات الكيميائية
مواد
- تفاح أو موز أو كمثرى
- عصير ليمون أو برتقال
- قرص فيتامين سي
كيف تصنع
- اختر واحدة من الثمار الثلاث وقم بتقطيعها إلى 3 أجزاء متساوية.
- ستكون القطعة الأولى بمثابة مقارنة مع القطع الأخرى. لذلك لا تضيف أي شيء إليها ، فقط اتركها مكشوفة للهواء.
- في إحدى القطع ، قم بتقطير محتويات ليمونة أو برتقالة. انتشر بحيث يتم تغطية كامل الفاكهة من الداخل بالعصير.
- في الجزء الأخير ، انشر فيتامين سي ، يمكن أن يكون قرصًا مطحونًا ، في جميع أنحاء لب الفاكهة.
- شاهد ما يحدث وقارن النتائج.
نتيجة
يجب أن يغمق لب الثمرة التي تعرضت للهواء بسرعة. يجب أن يبطئ عصير الليمون أو البرتقال وفيتامين ج ، وهي مادة كيميائية تسمى حمض الأسكوربيك ، من تحول لون الفاكهة إلى اللون البني.

تفسير
عندما نقطع الفاكهة ، تتلف خلاياها وتطلق إنزيمات مثل بوليفينول أوكسيديز ، والتي في يؤدي التلامس مع الهواء إلى أكسدة المركبات الفينولية الموجودة في الطعام ويسبب اللون البني الإنزيمي.
لمنع عمل الأكسجين ، يتم استخدام المواد الحافظة مثل حمض الأسكوربيك لأنها تتأكسد بشكل تفضيلي بدلاً من المركبات الفينولية. بالإضافة إلى قرص فيتامين سي ، يوجد حمض الأسكوربيك أيضًا في المصادر الطبيعية ، مثل الحمضيات والليمون والبرتقال ، المقترحة في التجربة.
تعلم المزيد عن أكسدة.
التجربة الثالثة - من يتجمد بشكل أسرع؟
المفاهيم المتضمنة: الخصائص التجميعية والتنظير بالتبريد
مواد
- أنبوبان (يستخدمان لمفضلات الحفلات)
- إناء زجاجي
- ملح الطعام
- مياه مصفاة
- جليد
- ميزان الحرارة
كيف تصنع
- أضف نفس الكمية من الماء المصفى إلى كلا الأنبوبين. على سبيل المثال ، 5 مل في كل أنبوب.
- أضف ملح الطعام إلى أحد الأنابيب وضع شريط تعريف لتمييز أيهما مالح.
- املأ الوعاء الزجاجي بالثلج المسحوق وأضف بعض الملح.
- ضع الأنبوبين في نفس الوقت داخل الجليد وراقب ما يحدث.
- سجل درجة حرارة التجمد لكل حالة.
نتيجة
تؤدي إضافة المذاب إلى الماء إلى خفض درجة حرارة التجمد. لذلك ، يميل الماء العادي إلى التجمد بشكل أسرع بكثير من محلول الملح والماء عند تعرضه لنفس الظروف.
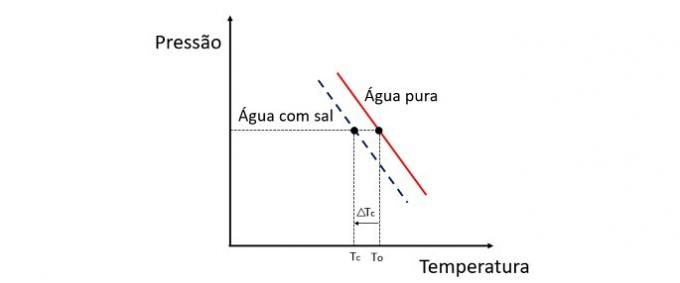
تفسير
Cryoscopy هي خاصية تجميعية تدرس التباين في درجة حرارة المذيب عند إذابة كميات مختلفة من المذاب فيه.
انخفاض درجة حرارة الماء المتجمد ناتج عن مادة مذابة غير متطايرة وهذه الظاهرة لها العديد من التطبيقات العملية. لذلك ، كلما زاد تركيز المذاب في المحلول يؤثر على تأثير التجميد.
على سبيل المثال ، إذا تجمد الماء عند 0 درجة مئوية وقمنا بإضافة الملح إليه ، فإن درجة حرارة تغير الطور ستكون سالبة ، أي أقل بكثير.
هذا هو السبب في أن مياه البحر لا تتجمد في الأماكن التي تقل درجة حرارتها عن 0 درجة مئوية. يميل الملح المذاب في الماء إلى خفض درجة حرارة التجمد. في الأماكن التي يوجد بها ثلوج ، من الشائع أيضًا إلقاء الملح على الطرق لإذابة الجليد وتجنب الحوادث.
تعلم المزيد عن الخواص التجميعية.
التجربة الرابعة - تحلل بيروكسيد الهيدروجين
المفاهيم المتضمنة: التفاعل الكيميائي والمحفز
مواد
- نصف حبة بطاطا نيئة ونصف مطبوخة
- قطعة كبدة نيئة وقطعة أخرى مطبوخة
- بيروكسيد الهيدروجين
- 2 طبق
كيف تصنع
- في كل طبق يضاف الطعام والبطاطس معا والكبد معا
- أضف 3 قطرات من بيروكسيد الهيدروجين في كل مادة من المواد الأربعة.
- شاهد ما يحدث وقارن النتائج.
نتيجة
عندما يتلامس بيروكسيد الهيدروجين ، وهو محلول بيروكسيد الهيدروجين ، مع الأطعمة النيئة ، يبدأ فورًا على الفور تقريبًا.
يمكن أيضًا إجراء هذه التجربة عن طريق إضافة قطعة من الطعام إلى وعاء به بيروكسيد الهيدروجين لجعل التفاعل أكثر وضوحًا.
تفسير
إن الفوران الناتج عن بيروكسيد الهيدروجين عند ملامسته للأطعمة النيئة يميز حدوث تفاعل كيميائي ، وهو تحلل بيروكسيد الهيدروجين وإطلاق الغاز الأكسجين.
يحدث تحلل بيروكسيد الهيدروجين من خلال عمل إنزيم الكاتلاز الموجود في عضية البيروكسيسومات الموجودة في الخلايا الحيوانية والنباتية.
من المهم ملاحظة أن تحلل بيروكسيد الهيدروجين يحدث تلقائيًا في وجود ضوء الشمس ، ولكن في تفاعل بطيء جدًا. ومع ذلك ، يعمل الكاتلاز كمحفز ، مما يزيد من سرعة التفاعل الكيميائي.
يمكن أن يكون بيروكسيد الهيدروجين مادة سامة للخلايا. لذلك ، يحلل الكاتلاز المركب وينتج الماء والأكسجين ، وهما مادتان لا تضر الجسم.
عند طهي الطعام ، تتغير مكوناته. التعديلات التي يسببها الطهي تؤثر أيضًا على عمل الكاتلاز عن طريق تغيير طبيعة البروتين.
نفس الإجراء الذي نراه مع الطعام هو ما يحدث عندما نضع بيروكسيد الهيدروجين على الجرح. يعمل الكاتلاز وهناك تكوين الفقاعات التي تتكون من إطلاق الأكسجين.
تعلم المزيد عن تفاعلات كيميائية.
مراجع ببليوغرافية
سانت ، و. ل. ص ؛ مول ، ج. س. (كوردس). كيمياء المواطن. 1. إد. ساو باولو: الجيل الجديد ، 2011. الخامس. 1, 2, 3.
الجمعية الكيميائية البرازيلية (منظمة) 2010. الكيمياء بالقرب منك: تجارب منخفضة التكلفة للفصل الدراسي من رياض الأطفال وحتى الصف الثاني عشر. 1. إد. ساو باولو.


