كما هو موضح في النص تفاعلات الإضافة، تحدث هذه التفاعلات العضوية عادةً مع المركبات التي لا تشبع (روابط مزدوجة أو ثلاثة أضعاف) ، حيث يتم كسر رابطة pi ، مما يسمح بدخول الذرات أو مجموعات الذرات في السلسلة. فحمي.
ومع ذلك ، فإن هذا النوع من التفاعل يحدث أيضًا في حالة ألكانات حلقي (هيدروكربونات مغلقة السلسلة مع روابط مشبعة (بسيطة) فقط بين ذرات كربون) التي تحتوي على ثلاث أو أربع ذرات كربون. لاحظ المثال أدناه ، وهو المعالجة بالبروم (تفاعل الهالوجين) من البروبان الحلقي:
CH2
/ \ + ر2 → ر CH2 CH2 CH2 ─ ر
ح2C CH2
وبالمثل ، هناك أيضًا تفاعل الإضافة المسمى بالهالوجين المائي أو إضافة الهاليد ، كما هو موضح أدناه:
CH2
/ \ + HBr → ح CH2 CH2 CH2 ─ ر
ح2C CH2
لاحظ أنه في كلتا الحالتين ، تم كسر الجزيء وتم إنتاج مركبات مفتوحة السلسلة.
لكن لا يحدث هذا بسهولة في الألكانات الحلقية التي تحتوي على خمس ذرات كربون أو أكثر. من ناحية أخرى ، من المرجح أن تعمل هذه المركبات تفاعلات الاستبدال، حيث لا يتم كسر الرابطة ، ولكن يتم استبدال ذرة أو أكثر من ذرات الهيدروجين المرتبطة بالكربون بذرات من عناصر أخرى.
لا يزال بإمكان السيكلوبنتان إجراء تفاعلات إضافة ، ولكن فقط عند درجات حرارة أعلى (حوالي 300 درجة مئوية). في حالة الهكسان الحلقي ، هذا صعب للغاية. ما يفعله في الواقع هو تفاعلات بديلة ، مثل الكلورة التالية:
CH2 CH2
/ \ / \
ح2C CH2 ح2C CH ─ Cl
│ │ + Cl2→ │ │ + H.Cl
ح2C CH2 ح2C CH2
\ / \ /
CH2 CH2
لا تتفاعل الحلقات التي تحتوي على خمس ذرات كربون أو أكثر مع الأحماض المائية ، مثل HBr ، بالإضافة إلى التفاعلات.
لكن لماذا يحدث هذا؟ لماذا تقوم الألكانات الحلقية المكونة من ثلاثة أو أربعة كربون بتفاعلات إضافة بينما لا تميل الألكانات الحلقيّة مع المزيد من ذرات الكربون إلى القيام بذلك؟
حسنًا ، هذا لأن السيكلوبروبان والسيكلوبوتان أكثر عدم استقرارًا ، لذلك من السهل كسر روابطهما.
يوهان فريدريش أدولف فون باير (1835-1917)
لتفسير ذلك ، قام الكيميائي الألماني يوهان فريدريش أدولف فون باير (1835-1917) بتطوير ما يسمى بـ نظرية الإجهاد الدائريالذي أظهر ذلك ستكون الروابط الأربعة التي تصنعها ذرات الكربون أكثر ثباتًا عندما يكون لها زاوية تساوي 109º 28 'كما هو الحال مع الميثان التالي:

روابط الميثان الأربعة المفردة بزاوية 109º 28 '
هذه هي الزاوية الأكثر استقرارًا لأنها تتوافق مع أكبر مسافة ممكنة بين الذرات في هندسة رباعية السطوح. بهذا ، يصبح التنافر الإلكتروني (التنافر بين الإلكترونات في طبقات التكافؤ للذرات) أصغر.
ألكانات حلقيّة تحتوي على ثلاثة وأربعة وخمسة كربون لها زوايا رابطة بين ذرات الكربون أقل من 109 º 28 '. نظرة:
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
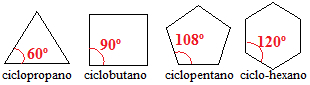
زوايا روابط الألكان الحلقي
بناءً على هذه الزوايا الحقيقية ، والتي يمكننا تسميتها بشكل عام α ، يمكن إجراء حساب إجهاد السندات باستخدام الصيغة التالية:
التوتر = 109º 28' - α
2
نحن نعلم أن البروبان الحلقي هو الأكثر اضطرابًا وأيضًا أكثر الألكان الحلقي تفاعلًا ، وهذا ما يتم تأكيده من خلال حساب جهد حلقته مقارنة بالآخرين:
الجهد السيكلوبروبان = 109º 28' – 60º = 109º – 60º + 28' = 49º + 28' = 24,5º + 14
2 2 2
0.5º = 30 ، إذن لدينا:
جهد البروبان الحلقي = 24º + 30 '+ 14' = 24º 44'
الجهد cyclobutane = 109º 28' – 90º = 9º 44'2
الجهد السيكلوبنتان = 109º 28' – 108º = 0º 44'2
وفقًا لنظرية باير للتوترات ، كلما زاد هذا التوتر ، زاد عدم استقرار دورة التدوير ، أي كلما زاد الفرق بين الزاوية الحقيقية (α) والزاوية النظرية (109º 28 ') ، أكثر استقرارًا ، وبالتالي ، سيكون رد الفعل أكثر مستوى.
هذا هو السبب في أن السيكلوبروبان هو الأقل استقرارًا من الألكانات الحلقية.
ومع ذلك ، كان هناك خطأ في نظرية باير ، لأنه إذا واصلنا القيام بحساب الإجهاد هذا للهكسان الحلقي ، عندما تكون زاوية الاتصال 120 درجة ، سنرى أن القيمة ستكون أصغر حتى من قيمة البروبان الحلقي ، مما يعطي مساويًا لـ -5 ° 16 '. قد يشير هذا إلى حقيقة أن الهكسان الحلقي يجب أن يكون غير مستقر أكثر وأن يقوم بردود فعل إضافة ، وهذا ليس هو الحال في الممارسة العملية.
تم العثور على تفسير هذه الحقيقة ، في عام 1890 ، من قبل الكيميائي الألماني هيرمان ساش ، وثبت في عام 1918 من قبل الكيميائي الألماني إرنست موهر. وفقًا لهؤلاء العلماء ، يكمن الخطأ في نظرية إجهاد حلقة باير في حقيقة أنه اعتبر أن جميع الألكانات الحلقية متحد المستوى ، أي أن جميع ذرات الكربون في مستوى واحد ، شاركاستخدم رسومات هياكلها الموضحة أعلاه.
ومع ذلك ، في الواقع ، حلقات الألكانات الحلقية التي تحتوي على أكثر من خمس ذرات كربون ليست مسطحة ، ولكن ذراتها. الحصول على المطابقات المكانية التي تلغي التوترات بين الاتصالات ، وإنشاء زاوية 109º 28 'بين روابط.
على سبيل المثال ، انظر إلى حالة الهكسان الحلقي. إنه في الواقع ليس مسطحًا بزاوية 120 درجة بين روابطه ، ولكن في الواقع ، ذراته "تدور" ، وتشكل شكلين محتملين ، شكل "الكرسي" و "القارب":
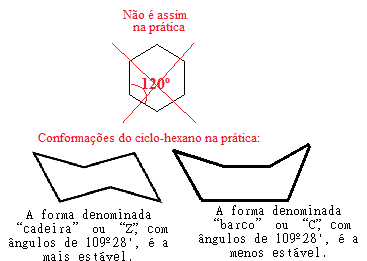
المطابقة الممكنة للهكسان الحلقي في الممارسة
لاحظ أنه نظرًا لأن الزاوية الحقيقية للهكسان الحلقي تساوي 109º 28 '، فهو مركب مستقر جدًا ، لذلك لا ينكسر جزيئه ، وبالتالي لا يشارك في تفاعلات الإضافة. لاحظ أيضًا أن شكل "الكرسي" هو الأكثر ثباتًا ، وهو الشكل الذي يسود دائمًا في الخلطات ، هذا لأنه ، في هذا التشكل ، تكون ذرات الهيدروجين المرتبطة بالكربون بعيدة عن بعضها البعض. الآخرين.
بقلم جينيفر فوغاسا
تخرج في الكيمياء