ال الضغط الاسموزي إنها خاصية جماعية تتوافق مع الضغط الذي يجب أن يمارس على نظام لمنع حدوث التناضح بشكل عفوي.
التناضح هو مرور الماء من وسط أقل تركيزًا (منخفض التوتر) إلى وسط أكثر تركيزًا (مفرط التوتر) عبر غشاء شبه نافذ حتى الوصول إلى التوازن.
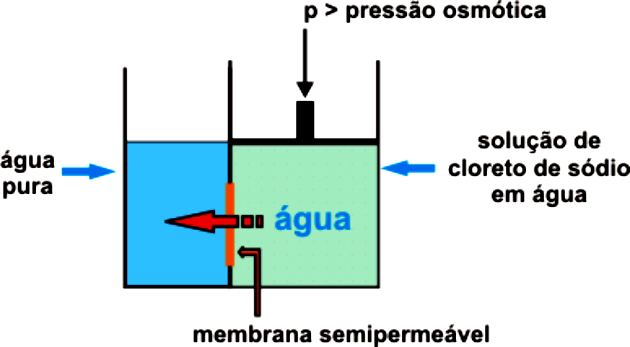
لمنع حدوث التناضح بشكل طبيعي ، من الضروري تطبيق ضغط خارجي على المحلول الأكثر تركيزًا ، مما يمنع مرور المذيب إلى الوسط الأكثر تركيزًا. هذا هو الضغط الأسموزي.
كلما زاد تركيز المحلول ، يجب أن يكون الضغط الأسموزي أكبر. لذلك ، فإن الضغط الاسموزي يتناسب مع تركيز الذائبة.
كيف تحسب الضغط الاسموزي؟
كل حل له قيمة ضغط أسموزي مختلفة. يمكن حساب الضغط الاسموزي من الصيغة التالية:
π = م. أ. ت. أنا
حيث لدينا المتغيرات التالية:
π = الضغط الاسموزي.
M = التركيز في مول / لتر ؛
R = ثابت غاز عالمي ، تقابل قيمته 0.082 ضغط جوي. ل. مول-1. ك-1 أو 62.3 مم زئبق. مول-1. ك-1;
T = درجة الحرارة على المقياس المطلق (كلفن) ؛
i = عامل Van't Hoff ، والذي يشتمل على العلاقة بين العدد الإجمالي للجسيمات النهائية والأولية في المحاليل الأيونية.
تمرين يحل
1. (Puccamp-SP) في بعض الأحيان ، يتم استخدام محلول الجلوكوز 0.30 M في الحقن الوريدي ، حيث يحتوي على ضغط تناضحي قريب من ضغط الدم. ما هو الضغط الأسموزي ، في الغلاف الجوي ، للمحلول المذكور عند 37 درجة مئوية؟
أ) 1.00.
ب) 1.50.
ج) 1.76.
د) 7.63.
هـ) 9.83.
بالنظر إلى البيانات التي يوفرها السؤال ، لدينا:
م = 0.30 مول / لتر ؛
R = 0.082 أجهزة الصراف الآلي. ل. مول -1. K-1
T = 37 درجة + 273 = 310 كلفن
يجب عليك الآن تطبيق هذه القيم على معادلة حساب الضغط الاسموزي:
π = م. أ. ت. أنا
π = 0,30. 0,082. 310
π = 7.63 ضغط جوي (لبديل)
تصنيف الحلول
يمكن تصنيف المحاليل إلى ثلاثة أنواع حسب الضغط الاسموزي:
- محلول مفرط التوتر: لديه ضغط أسموزي أعلى وتركيز مذاب.
- محلول متساوي التوتر: عندما يكون للحلول نفس الضغط الاسموزي.
- محلول ناقص التوتر: لديه ضغط أسموزي منخفض وتركيز مذاب.

أهمية الضغط الأسموزي للكائنات الحية
المحلول الملحي هو مادة محضرة على أساس مبادئ الضغط الاسموزي. يجب أن يطبق تحت ضغط تناضحي مساوٍ للضغط الموجود في الجسم ، فهذا يمنع خلايا حمراء لا تعاني من انحلال الدم أو تذبل.
يبلغ الضغط الأسموزي للدم حوالي 7.8 ضغط جوي. لذلك ، من أجل الأداء الصحيح للكائن الحي ، يجب أن يكون لخلايا الدم الحمراء نفس الضغط الاسموزي ، مما يضمن التدفق الطبيعي للماء داخل وخارج الخلايا.
في حالات الجفاف ، على سبيل المثال ، يشار إلى استخدام محلول ملحي ، والذي يجب أن يكون متساوي التوتر بالنسبة لخلايا الدم وسوائل الجسم الأخرى.
يقوم المحلول الملحي بوظيفة إعادة التوازن الأسموزي داخل الجسم. هذا لأنه أثناء الجفاف ، يصبح الدم أكثر تركيزًا من داخل الخلايا ، مما يؤدي إلى ذبولها.
التناضح والتناضح العكسي
كما رأينا ، فإن التنافذ إنها عملية تمرير الماء من منخفض التوتر إلى بيئة مفرطة التوتر ، من خلال غشاء شبه منفذ ، حتى يتم الوصول إلى التوازن بين التركيزات.
وفي الوقت نفسه ، فإن التناضح العكسي إنها عملية فصل المواد من خلال غشاء يحتفظ بالمذاب. يتدفق المذيب من الوسط الأكثر تركيزًا إلى الوسيط الأقل تركيزًا ويتم عزله عن المذاب بواسطة غشاء يسمح بمروره.
يحدث هذا فقط بسبب الضغط الذي يمارس ، مما يجعل الغشاء شبه المنفذ يسمح فقط بمرور الماء ، مع الاحتفاظ بالمذاب. يجب أن يكون هذا الضغط أكبر من الضغط الاسموزي الطبيعي.
على سبيل المثال ، إذا كان الضغط الأسموزي المطبق أكبر من اللازم ، فسيحدث التناضح العكسي. وبالتالي ، سوف يمر التدفق من الوسط ذي التركيز الأعلى إلى الوسيط ذي التركيز الأقل.



