تتضمن تفاعلات الأكسدة والاختزال نقل الإلكترونات بين الذرات أو الأيونات أو الجزيئات.
في تفاعل الأكسدة والاختزال ، تحدث تغيرات في رقم الأكسدة (أكسيد النيتروجين). تتكون الأكسدة من عمليات الأكسدة والاختزال:
- أكسدة: النتائج في فقدان الإلكترون وزيادة أكاسيد النيتروجين.
- تخفيض: النتائج في كسب الإلكترون ونقص أكاسيد النيتروجين.
عندما يتخلى أحد العناصر عن الإلكترونات ، سيستقبلها عنصر آخر. وبالتالي ، فإن العدد الإجمالي للإلكترونات المستلمة يساوي إجمالي عدد الإلكترونات المفقودة.
أمثلة على تفاعلات الأكسدة والاختزال للاحتراق والتآكل والتمثيل الضوئي.
أمثلة
اعتمادًا على العنصر الذي يتلقى أو يتبرع بالإلكترونات ، لدينا الأسماء التالية:
- الحد من وكيل: الذي يتعرض للأكسدة يسبب تقليله ويزيد من عدد أكاسيد النيتروجين. إنه ما يفقد الإلكترونات.
- عامل مؤكسد: الذي يخضع للاختزال يسبب الأكسدة ويقلل من عدد أكاسيد النيتروجين. هذا ما يكتسب الإلكترونات.
ا عدد التأكسد يمثل الشحنة الكهربائية لعنصر ما في الوقت الذي يشارك فيه رابطة كيميائية.
هذا الشرط مرتبط بـ كهرسلبيةوهو ميل بعض العناصر لاستقبال الإلكترونات.
1. لاحظ المثال الأول ، لاحظ أنه في التفاعل بين الحديد والكلور هناك تغيير في رقم الأكسدة. ا
الكلور لأنه أكثر كهرسلبية فإنه يكتسب إلكترونات: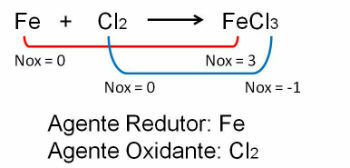
2. التفاعل بين الحديد والأكسجين. الأكسجين أكثر كهرسلبية وينتهي به الأمر بتلقي الإلكترونات وتقليل عدد تأكسدها.
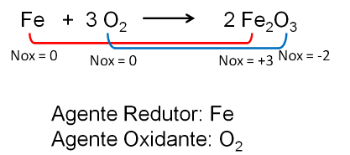
تعرف على المزيد ، اقرأ أيضًا:
- أكسدة
- الإحتراق
- تفاعلات كيميائية
- الإلكترونات
تمرين يحل
1. (PUC-RS) فيما يتعلق بمعادلة الأكسدة - اختزال غير متوازن Fe0 + CuSO4 → Fe2(فقط4)3 + نحاس0يمكن القول أن:
أ) عدد أكسدة النحاس في كبريتات النحاس هو +1.
ب) تفقد ذرة الحديد إلكترونين.
ج) النحاس يخضع للأكسدة.
د) الحديد عامل مؤكسد.
ه) الحديد يخضع للأكسدة.
القرار:
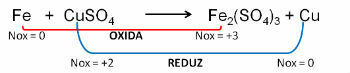
رد:
ه) الحديد يخضع للأكسدة.
تمارين
1. (UFAC-AC) في المعادلة الكيميائية التالية: Zn + 2 HCℓ → ZnCℓ2 + ح2
أ) يتأكسد عنصر Zn ويتفاعل كعامل مؤكسد.
ب) يتأكسد عنصر الزنك ويتفاعل كعامل اختزال.
ج) يقلل عنصر الزنك ويتفاعل كعامل اختزال.
د) HCℓ هو عامل مختزل.
هـ) تصنف المعادلة على أنها قابلة للعكس.
ب) يتأكسد عنصر الزنك ويتفاعل كعامل اختزال.
2. (ITA-SP) في التفاعل الأيوني Ni (s) + Cu2+(عبد القدير) → ني2+(عبد القدير) + النحاس (ق)
أ) النيكل هو عامل مؤكسد لأنه يتأكسد.
ب) النيكل هو المخفض لأنه يتأكسد.
ج) الأيون النحاسي هو مؤكسد لأنه يتأكسد.
د) الأيون النحاسي هو المخفض لأنه مخفض.
هـ) ليس رد فعل الأكسدة والاختزال ، وبالتالي لا يوجد مؤكسد أو مخفض.
ب) النيكل هو المخفض لأنه يتأكسد.
3. (UFRGS) العامل النشط في التبييض المنزلي هو أيون هيبوكلوريت ، ClO-. في عمليات التبييض ، يتم تقليل هذا الأيون ؛ هذا يعني ذاك:
أ) تستقبل المادة التي تخضع لعمل هيبوكلوريت الإلكترونات.
ب) هناك انخفاض في عدد الإلكترونات في بنيتها.
ج) ClO- هو عامل مختزل.
د) ClO- يتم تحويله إلى عنصر الكلور أو أيون الكلوريد.
ه) لا يحدث نقل الإلكترون.
د) ClO- يتم تحويله إلى عنصر الكلور أو أيون الكلوريد.


