التحليل الكهربائي هو أ تفاعل كيميائي غير تلقائي الذي ينطوي على تفاعل الأكسدة والاختزال ، والذي يحدث بسبب تيار كهربائي.
لكي يحدث التحليل الكهربائي ، يجب أن يكون التيار الكهربائي المعني مستمرًا وله جهد كافي.
لكي تتمتع الأيونات المعنية بالحرية في الحركة التي تؤديها ، يمكن أن يحدث التحليل الكهربائي عن طريق الاندماج (التحليل الكهربائي البركاني) أو عن طريق الانحلال (التحليل الكهربائي في المحلول).
تطبيقات التحليل الكهربائي
يتم إنتاج العديد من المواد والمركبات الكيميائية من عملية التحليل الكهربائي ، على سبيل المثال:
- الألمنيوم و نحاس
- هيدروجين و الكلور في الاسطوانة
- مجوهرات مقلدة (عملية الجلفنة)
- طنجرة الضغط
- عجلة المغنيسيوم (أغطية السيارة).
قوانين التحليل الكهربائي
تم تطوير قوانين التحليل الكهربائي بواسطة الفيزيائي والكيميائي الإنجليزي مايكل دي فاراداي (1791-1867). كلا القانونين يحكمان الجوانب الكمية للتحليل الكهربائي.
ال القانون الأول للتحليل الكهربائي لديه البيان التالي:
“تتناسب كتلة العنصر ، التي تترسب أثناء عملية التحليل الكهربائي ، طرديًا مع كمية الكهرباء التي تمر عبر الخلية الإلكتروليتية”.
س = أنا. ر
أين،
س: شحنة كهربائية (C)
أنا: شدة التيار الكهربائي (A)
ر: الفاصل الزمني لمرور التيار (التيار) الكهربائي
ال القانون الثاني للتحليل الكهربائي لديه البيان التالي:
“كتل العناصر المختلفة ، عند ترسيبها أثناء التحليل الكهربائي بنفس كمية الكهرباء ، تتناسب طرديًا مع معادلاتها الكيميائية”.
م = ك. و
أين،
م: مادة الكتلة
ك: ثابت التناسب
و: ما يعادل غرام من المادة
تعرف على المزيد في المقالة: ثابت فاراداي.
تصنيف
يمكن أن تحدث عملية التحليل الكهربائي من خلال الذوبان أو الذوبان:
التحليل الكهربائي الناري
التحليل الكهربائي الناري هو الذي تتم معالجته من إلكتروليت منصهر ، أي عن طريق عملية انصهار.
كمثال ، دعونا نستخدم كلوريد الصوديوم (كلوريد الصوديوم). عندما نقوم بتسخين المادة إلى 808 درجة مئوية ، فإنها تندمج وتوجد الأيونات (Na+ و Cl-) البدء في التمتع بحرية أكبر في الحركة ، في الحالة السائلة.
عندما التيار الكهربائي يمر في الخلية الإلكتروليتية ، الكاتيونات الصوديوم+ ينجذبهم القطب السالب المسمى الكاثود. بالفعل أنيون Cl-، بواسطة القطب الموجب ، أو الأنود.
في حالة نا+ يحدث تفاعل اختزال ، بينما في Cl-، هناك رد فعل أكسدة.
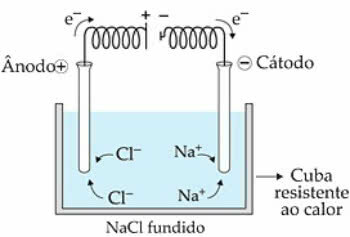
مخطط التحليل الكهربائي الناري كلوريد الصوديوم
التحليل الكهربائي المائي
في التحليل الكهربائي المائي ، المذيب المؤين المستخدم هو الماء. في محلول مائي ، يمكن إجراء التحليل الكهربائي باستخدام أقطاب كهربائية مقلوبة أو أقطاب كهربائية نشطة (أو تفاعلية).
أقطاب كهربائية خاملة: الماء في المحلول يتأين حسب المعادلة:
ح2يا ح+ + أوه-
مع ال التفكك من كلوريد الصوديوم لدينا:
NaCl → Na+ + Cl-
وهكذا ، فإن الكاتيونات H.+ و على+ يمكن تفريغها في القطب السالب ، بينما OH الأنيونات- و Cl- يمكن تفريغها في القطب الموجب.
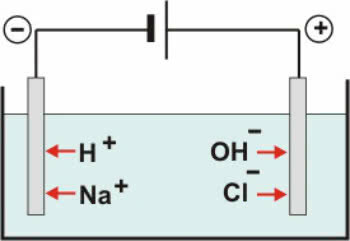
مخطط التحليل الكهربائي المائي كلوريد الصوديوم
يوجد في الكاتيونات تفاعل اختزال (اختزال كاثودي) ، بينما في الأنيونات يوجد تفاعل أكسدة (أكسدة أنوديك).
لذلك لدينا تفاعل التحليل الكهربائي:
2 كلوريد الصوديوم + 2 ح2O → 2 In+ + 2 أوه- + ح2 + Cl2
من هذا ، يمكننا أن نستنتج أن جزيئات NaOH تبقى في المحلول ، بينما H2 يتم تحريره في القطب السالب و Cl2، على القطب الموجب.
ستؤدي هذه العملية إلى المعادلة المكافئة:
2 كلوريد الصوديوم + 2 ح2O → 2 هيدروكسيد الصوديوم + H.2 + Cl2
الأقطاب الكهربائية النشطة: في هذه الحالة تشترك الأقطاب الكهربائية النشطة في التحليل الكهربائي ، ومع ذلك فإنها تعاني من التآكل.
على سبيل المثال ، لدينا التحليل الكهربائي في محلول مائي من كبريتات النحاس (CuSO4):
كوسو4 → نحاس2 + نظام التشغيل 2-4
ح2O → H.+ + أوه-
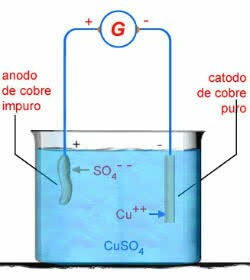 مخطط التحليل الكهربائي المائي CuSO4
مخطط التحليل الكهربائي المائي CuSO4
في هذه الحالة سوف يتآكل أنود النحاس:
الحمار0 → نحاس2+ + 2 هـ-
هذا لأنه وفقًا للإمكانات القياسية للأقطاب الكهربائية ، فإن التيار الكهربائي لديه وقت أسهل في إزالة الإلكترونات من النحاس0 من نظام التشغيل 2-4 أو من أوه-.
لذلك ، عند القطب السالب ، يحدث تفاعل التحليل الكهربائي التالي:
2 هـ- + نحاس2+ → نحاس
على القطب الموجب ، لدينا تفاعل التحليل الكهربائي:
نحاس ← نحاس2+ + 2 هـ-
أخيرًا ، عندما نضيف معادلتين للتحليل الكهربائي ، يصبح لدينا صفر نتيجة لذلك.
هل تريد معرفة المزيد عن الموضوع؟ اقرأ المقالات:
- أيون ، كاتيون وأنيون
- تفاعلات كيميائية
- تفاعلات الأكسدة
البطارية والتحليل الكهربائي
يعتمد التحليل الكهربائي على ظاهرة معكوسة لظاهرة البطارية. في التحليل الكهربائي ، لا تكون العملية تلقائية ، كما تحدث في البطاريات. بمعنى آخر ، يحول التحليل الكهربائي الطاقة الكهربائية إلى طاقة كيميائية ، بينما تولد الخلية الطاقة الكهربائية من الطاقة الكيميائية.
معرفة المزيد عن الكيمياء الكهربائية.
تمارين
1. (Ulbra-RS) يمكن إنتاج البوتاسيوم المعدني بواسطة التحليل الكهربائي البركاني لكلوريد البوتاسيوم. من هذا البيان ، حدد البديل الصحيح.
أ) التحليل الكهربائي هو عملية تتضمن تفاعلات تقليل الأكسدة والاختزال التي يحفزها التيار الكهربائي.
ب) يتم التحليل الكهربائي الناري لكلوريد البوتاسيوم في درجة حرارة الغرفة.
ج) يوجد البوتاسيوم في الطبيعة بالشكل المختزل (K0).
د) تفاعل التحليل الكهربائي هو تفاعل يحدث بمساعدة الأشعة فوق البنفسجية.
هـ) في عملية التحليل الكهربائي لكلوريد البوتاسيوم ، للحصول على البوتاسيوم المعدني ، يحدث انتقال الإلكترونات من البوتاسيوم إلى الكلور.
بديل ل
2. (UFRGS-RS) يوجد دائمًا في الكاثود لخلية التحليل الكهربائي:
أ) ترسب المعادن.
ب) اختزال نصف تفاعل.
ج) إنتاج التيار الكهربائي.
د) إطلاق غاز الهيدروجين.
هـ) التآكل الكيميائي.
البديل ب
3. (Unifor-CE) ترتبط المقترحات التالية بالتحليل الكهربائي:
أنا. تحدث تفاعلات التحليل الكهربائي مع استهلاك الطاقة الكهربائية.
ثانيًا. لا يمكن تحليل محاليل الجلوكوز المائية لأنها لا توصل تيارًا كهربائيًا.
ثالثا. في التحليل الكهربائي للمحاليل الملحية ، تخضع الكاتيونات المعدنية للأكسدة.
يمكننا أن نقول ذلك فقط:
أ) أنا على صواب.
ب) الثاني هو الصحيح.
ج) الثالث هو الصحيح.
د) الأول والثاني صحيحان.
هـ) الثاني والثالث صحيحان.
لبديل
4. (FEI-SP) قام اثنان من طلاب الكيمياء بإجراء التحليل الكهربائي BaCl2; الأول مائي والثاني ناري. فيما يتعلق بالنتيجة ، يمكننا القول أن كلاهما حصل على:
آه2 انها ال2 في الأنودات.
ب) ح2 وبا في الأنودات.
ج) Cl2 وبا على الأقطاب الكهربائية.
د) ح2 في الكاثودات.
ه) Cl2 في الأنودات.
بديل و
5. (فونيس) "تجمع بدون كيمياء"إعلان يتضمن معالجة المياه. ومع ذلك ، فمن المعروف أن العلاج يتكون من إضافة كلوريد الصوديوم إلى الماء وتمرير هذا الماء من خلال وعاء مجهز بأقطاب نحاسية وبلاتينية موصولة برصاص جمل.
أ) بناءً على هذه المعلومات ، ناقش ما إذا كانت الرسالة الإعلانية صحيحة
ب) بالنظر إلى الأقطاب الكهربائية الخاملة ، اكتب معادلات التفاعلات المتضمنة التي تبرر الإجابة السابقة.
أ) الرسالة الإعلانية غير صحيحة ، حيث سيكون هناك تكوين لمنتجات كيميائية.
ب) 2 كلوريد الصوديوم + 2 ح2O → 2 هيدروكسيد الصوديوم + H.2 + Cl2 (تفاعل مكون الكلور ، مفيد في معالجة مياه البركة)
2 هيدروكسيد الصوديوم + Cl2 → NaCl + NaClO + H2O (تفاعل يشكل NaClO ، مبيد جراثيم قوي)