تستخدم مصابيح الهالوجين (وتسمى أيضًا مصابيح الهالوجين) على نطاق واسع من قبل المتخصصين في الهندسة المعمارية والتصميم الداخلي لإنشاء بيئات مختلفة تتطلب المزيد من نقاط الإضاءة شديد.
هذه المصابيح لها نفس مبدأ التشغيل مثل المصابيح المتوهجة ، أي أنها تتشكل بشكل عام بواسطة أمبولة ذات خيوط رفيعة من التنجستن (W) ، معدن ذو نقطة انصهار عالية جدًا ، ومقاوم للارتفاع درجات الحرارة. عندما يتم عبور خيوط التنجستن بواسطة تيار كهربائي ، فإنها تصدر ضوءًا أبيض مع مسحة صفراء قليلاً.
بمرور الوقت ، يتصاعد التنغستن (يتغير من الحالة الصلبة إلى الحالة الغازية) من الفتيل والترسبات في المصباح ، مما يؤدي إلى تعتيم اللمبة:
دبليو(س) ↔ دبليو(ز)
ومع ذلك ، فإن الاختلاف بين المصابيح المتوهجة الشائعة ومصابيح الهالوجين هو أن الأخيرة تحتوي على اليود الغازي بالداخل. اليود هو من عائلة الهالوجينات في الجدول الدوري ، ومن هنا جاء الاسم الذي يطلق على هذا النوع من المصابيح.
في الفتيل ، يتفاعل اليود مع التنغستن الغازي الذي يتم إطلاقه ، مكونًا غاز يوديد التنجستن:
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
دبليو(ز) + 3 أنا2 (ز) ↔ WI6 (ز)
عندما يقترب هذا الغاز من البصلة ، وهي منطقة أكثر برودة ، فإنه يتحلل ، وبالتالي يستعيد التنجستن المعدني (الصلب) ، والذي يترسب مرة أخرى على الفتيل.
WI6 (ز) ↔ دبليو(س) + 3 أنا2 (ز)
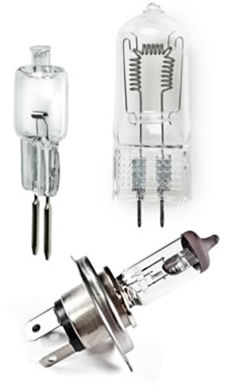
والنتيجة هي أن هذا النوع من المصابيح لا يخفت ويستمر لفترة أطول. تدوم المصابيح المتوهجة العادية لمدة عام أو 1000 ساعة في المتوسط ، بينما تدوم مصابيح الهالوجين 2000 ساعة ويمكن أن تصل إلى 5000 ساعة. كما أنها أكثر كفاءة أو اقتصادية من تلك المتوهجة. لكن من الجدير بالذكر أنهم يستهلكون طاقة أكثر مقارنةً بالفلوريسنت أو التفريغ.
هذه النقاط وحقيقة أن ضوءها أكثر إشراقًا من المتوهج العادي هو ما يجعل استخدامه ينمو أكثر فأكثر.
أحد أنواع مصابيح الهالوجين هو المصباح ثنائي اللون ، والذي يحتوي على عاكس يقلل من الحرارة الزائدة الناتجة.
بقلم جينيفر فوغاسا
تخرج في الكيمياء
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
فوغا ، جينيفر روشا فارغاس. "التوازن الكيميائي في مصابيح الهالوجين" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/equilibrio-quimico-lampadas-halogenas.htm. تم الوصول إليه في 28 يونيو 2021.
كيمياء

اختبر معلوماتك وتعلم المزيد مع هذه القائمة من التمارين التي تم حلها على الموازين الكيميائية. من خلال هذه المادة ، ستكون قادرًا على فهم كيفية عمل ثوابت التوازن (Kp و Kc و Ki) بشكل أفضل ، وتحول التوازن ، ودرجة الحموضة و pOH ، وكذلك التوازن في ما يسمى بالحلول العازلة.