Реакції окислення-відновлення, що відбуваються в присутності перекису водню (водний розчин перекису водню - H2О2 (вод.)) становлять особливий випадок, який потрібно аналізувати окремо, головним чином щодо його балансу. Це пов’язано з тим, що кисень у пероксиді водню, у якому Nox дорівнює -1, може або окислюватися, або відновлюватися.
Наприклад, давайте розглянемо два випадки, коли він поводиться спочатку як окислювач (відновник), а потім як відновник (окислювач):
- окислювач: всякий раз, коли перекис водню відновлюється, діючи як окислювач, він утворює воду як продукт.
Якщо до розчину, що містить йодид-іони, додати розчин перекису водню (I-) в кислому середовищі ми матимемо:
H2О2 (вод.) + Я-(тут) + H+(тут) → H2О(1) + Я2 (s)
Дивіться, що утворюються вода та йод. Але щоб перевірити, чи дійсно пероксид водню діяв як окислювач і відновлювався, спостерігайте за визначенням ступенів окислення (NOx): *

Кисень Nox перекису водню зменшився з -1 до -2, враховуючи, що він отримав 1 електрон. Однак, оскільки ми маємо два кисню в кожній молекулі пероксиду водню (H2О2), варіація Nox буде дорівнювати 2.
Отже, як показано в тексті “Окисно-відновне балансування”, Необхідним кроком для збалансування реакцій методом окисно-відновного є інвертування значень варіацій Nox за коефіцієнтами, будучи, в даному випадку, наступним чином:
* H2О2 = 2 (∆Nox) = 2 → 2 буде коефіцієнтом I-;
* Я-= ∆Nox = 1 → 1 буде коефіцієнтом H2О2.
Таким чином, ми маємо:
1 год2О2 (вод.) + 2 I-(тут) + H+(тут) → H2О(1) + Я2 (s)
Досягнення інших коефіцієнтів шляхом балансування за випробуваннями:
- Оскільки в першому елементі є два атоми кисню, коефіцієнт води у другому члені повинен дорівнювати 2. А оскільки в 1-му члені також є два йодид-іони, то коефіцієнт йоду у 2-му члені буде 1. Не забувайте, що нам потрібно помножити індекс на коефіцієнт, щоб знайти правильну кількість атомів та іонів у кожному члені:
1 год2О2 (вод.) + 2 I-(тут) + H+(тут) → 2 год2О(1) + 1 I2 (s)
Не зупиняйтесь зараз... Після реклами є ще щось;)
- Тепер залишається лише збалансувати катіон водню 1-го члена, і його коефіцієнт повинен бути рівним 2, оскільки у 2-му члені він має 4 водню, а в 1-му - 2:
1 год2О2 (вод.) + 2 I-(тут) +2 год+(тут) → 2 год2О(1) + 1 I2 (s)
- відновник: всякий раз, коли перекис водню окислюється, діючи як відновник, він утворює кисень (O2) як продукт.
Прикладом зменшення перекису водню є контакт із перманганатом калію (KMnO4). Ця речовина має дуже характерний фіолетовий колір, але при контакті з перекисом водню вона стає безбарвною. Це пов’язано з тим, що весь марганець присутній в іоні MnO4- розчину перманганату відновлюється, утворюючи іон Mn2+, як показано нижче:
+1 -1 +7 -2 +1 0 +2 +1 -2
H2О2 + MnO4-+ H+ → The2 + Мн2++ H2О
Розраховуючи Nox, ми бачимо, що кисень у пероксиді водню насправді окислює і спричинює відновлення марганцю:
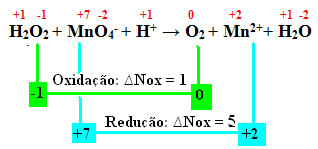
Як і в попередньому прикладі, oxНокс перекису водню буде дорівнює 2, оскільки є два кисню, і кожен втрачає електрон. Тому ми маємо:
* О2 = 2 (∆Nox) = 2 → 2 буде коефіцієнтом MnO4-;
* MnO4- = ∆Nox = 5 → 5 буде коефіцієнтом O2.
І як усі O2 походить від перекису водню, дві речовини мають однаковий коефіцієнт:
5 H2О2 + 2MnO4-+ H+ → 5 О2 + Мн2++ H2О
Балансуючи методом проб, ми маємо:
5 годин2О2 + 2 MnO4-+ 6 год+ → 5 O2 + 2 млн2++ 8 год2О
* Для будь-яких питань про те, як розрахувати число окислення (Nox) атомів та іонів у реакції, прочитайте текст “Визначення числа окислення (Nox)”.
Дженніфер Фогача
Закінчив хімію
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. "Окисно-відновлювальні реакції із залученням пероксиду водню"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao-envolvendo-agua-oxigenada.htm. Доступ 28 червня 2021 року.


