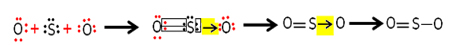
Коли бензольне кільце вже має заступник, цей радикал впливатиме на всі інші заміни Н на кільці. Цей замінник може бути орто і парарежисером або метарежисером. Але виникають питання:
| Що змушує групу, прикріплену до бензольного кільця, впливати на напрямок та реакційну здатність реакції заміщення? |
| Що робить певні групи цільовими радниками (відключення), а інші орто-пара (активізацію)? |
На ці два запитання відповідає розуміння покликань. електронні ефекти що ці групи здійснюють на рингу. Цей ефект виникає через різниця електронегативності між елементами, як заступник поляризують зв’язки ароматичного ядра, по черзі індукуючи позитивний характер до деяких вуглецевих кільцях, тоді як інші залишаються з негативним.
| Нове заміщення відбудеться в атомах вуглецю, що мають характер негативний. |
Давайте подивимося, як ці електронні ефекти відбуваються в ароматичному кільці, маючи на увазі порядок електронегативності елементів: F> O> N> Cl> Br> S> C> I> H.
1-й випадок: радикальна активація або орто-до режисера:
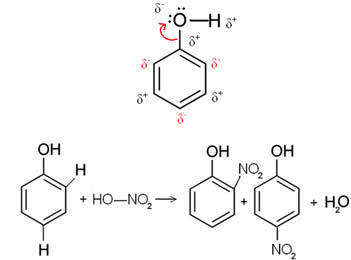
Наприклад, у випадку нижче молекули бензолу (фенолу) кисень є найбільш електронегативним елементом, отже він притягує до себе електрони, змушуючи вуглець мати частково позитивний заряд, який індукує змінна кільцева поляризація. Позиції, які є від’ємними, - це саме орто і пара позиції. Ось чому група -OH є активуючим радикалом або орто-до-директорів. Це видно з реакції нітрування фенолу нижче, що призводить до о-нітрофенолу та р-нітрофенолу як продуктів:
Не зупиняйтесь зараз... Після реклами є ще щось;)
2-й випадок: дезактивація радикала або мета-лідера:
Тепер розглянемо випадок з нітробензолом:
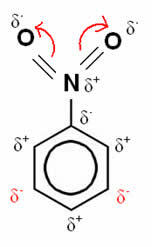
У цьому прикладі кисень залишається найбільш електронегативним елементом, тому він притягує до себе зв’язки, утворені з азотом, який частково позитивно заряджений, змушуючи приєднаний до нього атом вуглецю стати негативно поляризованим і так послідовно. Таким чином, позиція, яка стає негативною і найбільш сприйнятливою до заміщення, є позицією мета, будучи, отже, a відключення.
Побачте тепер детальніше цей електронний ефект, який називається резонансний ефект.
| резонансний ефект це притягання або відштовхування електронів на π (pi) зв’язках подвійних або потрійних зв’язків, коли вони резонують із самим бензольним кільцем. |
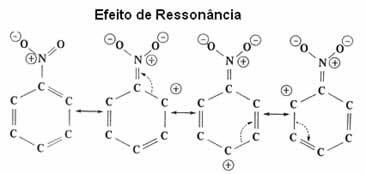
Як видно, група NO2 деактивує кільце, оскільки забирає з нього електрони і зменшує його електронну щільність. Таким чином, група, яка буде атакувати та робити заміщення (електрофіл), є позитивною, тому вона переважно атакує метапозицію, яка отримала негативний заряд.
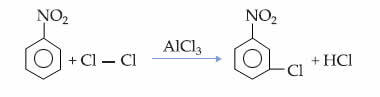
Цей факт можна побачити в реакції монохлорування нітробензолу, при якій заміщення відбувається лише в метаположенні:
Дженніфер Фогача
Закінчив хімію
Шкільна команда Бразилії
Хотіли б ви посилатися на цей текст у школі чи академічній роботі? Подивіться:
FOGAÇA, Дженніфер Роша Варгас. "Електронні ефекти радикалів мета та орто-до-директора"; Бразильська школа. Доступно: https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm. Доступ 28 червня 2021 року.