Старшокласники завжди піддаються облицюванню окисно-відновних реакцій з іони, як на вступних іспитах, так і на Національному іспиті середньої школи (Енем). Таким чином, балансування цих рівнянь може бути дуже страшною темою.
З метою полегшення розуміння цієї теми цей текст спрямований на збалансування окисно-відновних рівнянь з іонами з описом деяких кроків для його проведення. Для цього ми повинні розпочати з виявлення цього типу хімічної реакції.
В окисно-відновних реакцій з іонами ідентифікуються за наявністю одного або декількох компонентів із зарядами (позитивними чи негативними), тобто іони (катіони або аніони), які можуть бути присутніми в реагентах або продуктах, як у двох прикладах a дотримуйтесь:
1-й приклад:Кр2О72- + Fe2+ + H+ → Кр3+ + Fe3+ + H2О
2-й приклад:Кл2 + C + H2O → CO2 + H+ + Кл-
Для проведення балансуючи рівняння окисно-відновних реакцій з іонами, важливо виконати деякі кроки, такі як:
1-й крок: визначити NOX кожного з атомів реагентів і продуктів рівняння;
2-й крок: перевірити, які види страждали окислення;
3-й крок: визначте варіацію NOX вид, що зазнав окислення;
4-й етап: помножте варіації, виявлені на третьому етапі, на кількість атомів окислювальних видів;
5-й крок: перевірити, які види страждали скорочення;
6-й етап: визначити варіацію NOX у видів, що зазнали скорочення;
7-й етап: помножте варіації, виявлені на третьому етапі, на кількість атомів виду, яку він зменшує;
8-й крок: використовуйте значення, знайдене на четвертому етапі, як коефіцієнт виду, що зменшує;
9-й етап: використовуйте значення, знайдене на сьомому етапі, як коефіцієнт окислювальних речовин;
10-й крок: покладіть коефіцієнти в інші види, згідно з методом пробне балансування. У тих видах, де це неможливо, ставлять невідомі як коефіцієнти;
11-й крок: помножте коефіцієнт кожного виду на його навантаження;
12-й крок: зрівняйте суму зарядів реагентів із сумішшю продуктів, щоб знайти коефіцієнт одного з видів з невідомими;
13-й крок: складіть баланс, використовуючи пробний метод.
Для полегшення розуміння дотримуйтесь покрокового опису, описаного вище, у наступному прикладі a окисно-відновне рівняння з іонами:

Іонне рівняння, що показує деякі іони та загальні групи заряду 0
1-й крок: NOX кожного атома.

NOX атомів, присутніх у рівнянні
2-й крок: Види, що зазнають окислення.

Види, які зазнають окислення в рівнянні
Оскільки NOX йоду збільшується від -1 до 0 від реагенту до продукту, отже, окисненню піддається цей вид.
3-й крок: Визначте варіацію NOX окислених видів.
Для цього просто відніміть найбільший NOX за найнижчий NOX:
∆NOX = (0) – (-1)
∆ NOX = 0 + 1
∆ NOX = 1
Крок 4: Множення NOX на кількість.
На цьому етапі ми множимо варіації, виявлені на третьому етапі, на кількість атомів виду.
Я- = ∆NOX.1
Я- = 1.1
Я- = 1
5-й крок: Види, що зазнають скорочення.

Види, які зазнають зменшення рівняння
Оскільки NOX хрому зменшується від +7 до +3 від реагенту до продукту, отже, це речовина зазнає відновлення.
6-й крок: Визначте варіацію NOX у відновлених видах.
Для цього просто відніміть найбільший NOX за найнижчий NOX:
∆NOX = (+6) – (+3)
∆ NOX = +6 – 3
∆ NOX = 3
7-й крок: Множення NOX на кількість.
На цьому кроці ми множимо варіацію, виявлену на шостому кроці, на кількість атомів виду.
Кр2О72- = ∆NOX.1
Кр2О72- = 3.2
Кр2О72- = 6
8-й крок: Почніть балансувати.
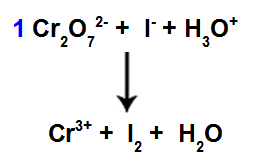
Початок балансування з використанням знайденого коефіцієнта
На цьому кроці ми починаємо балансування, розміщуючи коефіцієнт, знайдений на четвертому етапі у видів, які зазнали зменшення.
9-й крок: Продовжуйте балансування.

Продовження балансування з використанням знайденого коефіцієнта
10-й крок: Використовуйте пробний метод.
У реагенті 6 атомів I, тому ми повинні покласти коефіцієнт 3 у I-виду2 продукту, оскільки в ньому є лише 2 атоми Cl;
Як і у видів 1, Cr2О72-, є 2 атоми Cr, ми повинні покласти коефіцієнт 2 у виду Cr3+ товару.
Оскільки у нас є кисень у трьох видів, а у двох з них відсутні коефіцієнти, для продовження балансу ми повинні помістити невідомі в інші види:
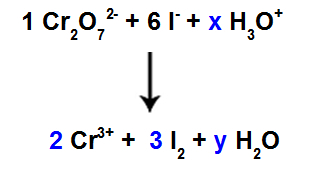
Коефіцієнти після використання пробного методу
11-й крок: Розмноження кожного виду на його навантаження.
Для цього просто помножте коефіцієнт виду на його навантаження, наступним чином:
В реагентах:
Кр2О72- = 1.(-2) = -2
Я- = 6.(-1) = -6
H3О+ = x. (+ 1) = + x
На продукцію:
Кр3+ = 2.(+3) = +6
Я2 = 4.0 = 0
H2O = y.0 = 0
12-й крок: Сума звинувачень.
На цьому кроці ми повинні додати завантажені реагенти та продукти, знайдені на кроці 11:
Реактиви = продукти
-2 + (-8) + (+ x) = +6 + 0 + 0
-2 - 6 + x = 6
-8 + x = 6
x = 6 + 8
х = 14
13-й крок: Кінець балансування.
Щоб завершити балансування, ми повинні:
Покладіть результат, знайдений на 12-му етапі у виду H3О+;
Оскільки зараз у нас у реагенті 42 атоми Н, необхідно помістити коефіцієнт 21 у Н-види2У продукті.
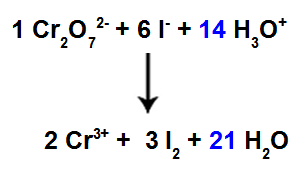
Рівняння збалансованої іонної реакції
Мені Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao-com-ions.htm

