
Кількість калорій залежить від конституції їжі. Отже, щоб експериментально визначити кількість тепла, яке виділяється їжею і яке може засвоїти організм, ми використовуємо пристрій, який називається калориметр.
Цей пристрій вимірює тепло, яке виділяється їжею при її спалюванні. Існує кілька типів калориметрів; перша з них була створена в 1780 р. Лавуазьє та Лапласом і була льодовий калориметр.
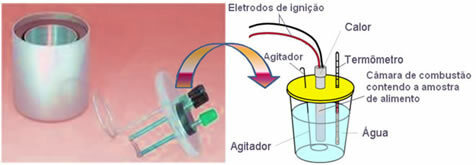
На сьогоднішній день найбільш вживаним, який враховує пояснювану вище концепцію калорій, є водний калориметр. Цей пристрій покритий ізоляційним матеріалом, щоб запобігти втратам тепла від середовища; і їжа, що підлягає аналізу, поміщається в камера згоряння, який містить газоподібний кисень і електроди. Ці електроди зазнають електричного розряду і спричиняють їх запалювання та згоряння їжі.
Відома маса води, що міститься в калориметрі, поглинає тепло, що виділяється спаленою їжею, а термометр вимірює підвищення температури води. Крім того, калориметр містить агітатор що дозволяє температурі води залишатися рівномірною протягом усієї своєї температури.
Отже, якщо ми використовуємо, наприклад, масу 1 грам цукру, а калориметр має 1000 г води, і ми спостерігаємо, що врешті-решт реакції температура води перейшла з 20 ° C до 24 ° C, тобто вона зросла на 4 ° C, тоді ми можемо досягти енергетичної цінності цукор. Подібно до? Ну, враховуючи початкову концепцію калорійності, ми маємо:
| Підняти від 1 ° C → 1 кал на грам води |
| Підняти від 4 ° C → 4 кал на грам води |
Так 1 г води поглинає 4 вапна. Однак було використано 1000 г води, і, враховуючи, що все тепло, що виділяється при згорянні, поглиналося нею, загальна енергія, поглинена водою, становила 4000 кал або 4 ккал. Тому ми робимо висновок, що:
| Енергетична цінність цукру = 4000 кал / г або 4 ккал / г. |
Перетворення на СІ:
1 ккал 4,18 кДж
4 ккал / г х
х = 16,72 кДж / г.
Крім того, ми можемо використовувати наступне рівняння для обчислення кількості теплоти, що віддається або поглинається водою:
| Q = m. ç. т |
Де:
Q = тепло, віддане або поглинене водою;
m = маса води;
c = питома теплоємність води, яка дорівнює 1,0 кал / г. ° C або 4,18 Дж / р. ° С;
Δt = зміна температури, яку зазнає вода, що визначається зменшенням кінцевої температури на початкову (tf - тi).
Використовуючи цю формулу, ми отримуємо той самий результат:
Q = m. ç. т
Q = 1000 г. 1,0 кал / г. ° С (24-20) ° С
Q = 4000 кал
Q = 4,0 ккал
або
Q = m. ç. т
Q = 1000 г. 4,18 кДж / г. ° С (24-20) ° С
Q = 16,72 кДж
Дженніфер Фогача
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/medindo-as-calorias-dos-alimentos-por-meio-um-calorimetro.htm
