Атом - це назва, дана формувачу речовини (усього, що займає простір і має масу). Цю назву запропонували грецькі філософи Демокріт і Левкіпп. Хімічні елементи, молекули, речовини а органічні або неорганічні матеріали утворені атомами.
У своїй конституції атом має частинки (протони, нейтрони та електрони), які не є найменшою частиною речовини. Тим не менше, ваша візуалізація неможлива. Те, що відомо про атом, пов’язане з науково доведеними фізичними, хімічними та математичними аспектами.
Еволюція знань про атом спричинила розробку та вдосконалення декількох технологій.
Основний склад атома
Ядро: щільніша область атома і містить протони та нейтрони;
Рівні енергії: регіони, що оточують ядро і містять підрівні, орбіталі та електрони. Існує сім рівнів енергії, які представлені буквами K, L, M, N, O, P і Q;
Підрівні енергії: є регіони, в яких розміщуються орбітали. Вони присутні на всіх рівнях і представлені буквами (s, p, d f). Його кількість залежить від кожного рівня: K (має s підрівнів), L (має s і p підрівнів), M (має s, p і d підрівнів), N (має підрівні s, p, d і f), O (має підрівні s, p, d і f), P (має підрівні s, p і d) і Q (має підрівні s і Р);
Атомні орбіталі: регіони, які найімовірніше знайдуть електрон. Кожен підрівень має різну кількість орбіталей: s (одна орбіталя), p (три орбіталі), d (п’ять орбіталей) і f (сім орбіталей);
протони: позитивні частинки (представлені р);
електрони: негативні частинки, які також мають хвильову поведінку (представлені е);
нейтрони: незаряджені частинки, що зменшують відштовхування між протонами в ядрі (представлені n).
Карта розуму: Атом
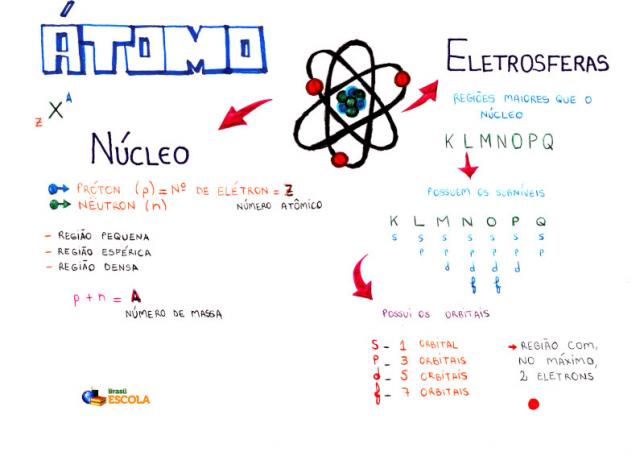
* Щоб завантажити карту розуму в PDF, Натисніть тут!
подання атома
Найпростіший спосіб представити атом - використовувати абревіатуру хімічного елемента, який він утворює. Наприклад, абревіатура Se представляє всі атоми, що утворюють хімічний елемент селен.
Абревіатура, що представляє атом, все ще може надати дві важливі відомості: атомний номер (представлений літерою Z і завжди з лівого боку внизу абревіатури атома) та масове число (представлене літерою A, яке можна розташувати зліва чи справа у верхній частині абревіатури атома атом).
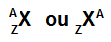
Скорочення атома з масовим числом та атомним номером
атомний номер (Z): позначає кількість протонів, присутніх в ядрі атома, і кількість електронів (e), присутніх на енергетичних рівнях.
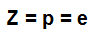
Формула, яка вказує на репрезентативність атомного номера
Масове число (A): позначає масу, присутню в ядрі атома, яка є результатом суми кількості протонів (p) та кількості нейтронів (n).

Формула, яка вказує на репрезентативність масового числа
Атомна подібність
Атоми одного і того ж хімічного елемента або різних хімічних елементів можна порівняти за кількістю протонів, електронів, нейтронів і маси, класифікуючи їх наступним чином:
а) Ізотопи
Вони є атомами, які мають:
той самий атомний номер;
стільки ж протонів;
різне масове число;
різну кількість нейтронів;
Приклад:
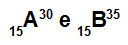
Атоми А і В є ізотопами
Атоми А і В є ізотопами, оскільки:
Атом А має 15 протонів, атомний номер дорівнює 15, 15 електронам, 15 нейтронам і масове число, що дорівнює 30.
Атом В має 15 протонів, атомний номер дорівнює 15, 15 електронам, 20 нейтронам і масове число, що дорівнює 35.
б) Ізобари
Вони є атомами, які мають:
різні атомні номери;
різну кількість протонів;
різну кількість електронів;
однакові масові числа;
різну кількість нейтронів.
Приклад:
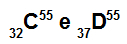
Атоми C і D є ізобарами
Атоми C і D є ізобарними, оскільки:
Атом С має 32 протони, атомний номер дорівнює 32, 32 електрони, 23 нейтрони і масове число, що дорівнює 55.
Атом D має 37 протонів, атомний номер дорівнює 37, 37 електронам, 18 нейтронам і масове число, що дорівнює 55.
в) Ізотони
Вони є атомами, які мають:
різні атомні номери;
різну кількість протонів;
різну кількість електронів;
різні масові числа;
стільки ж нейтронів.
Приклад:
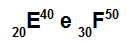
Атоми E і F є ізотопами
Атоми E і F є ізотопами, оскільки:
Атом Е має 20 протонів, атомний номер дорівнює 20, 20 електронам, 20 нейтронам і масовому числу, рівному 40.
Атом F має 30 протонів, атомний номер дорівнює 30, 30 електронам, 20 нейтронам і масове число, рівне 50.
г) Ізоелектроніка
Вони є атомами, які мають:
стільки ж електронів.
ПРИМІТКА: ізоелектронні атоми також можуть мати однакове масове число (ізобари), однакову кількість нейтронів (ізотонів) або однакову кількість протонів (ізотопів).
Приклад:
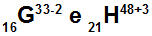
Атоми G і H є ізоелектронними
Атоми G і H є ізоелектронними, оскільки:
Атом G має 16 протонів, атомний номер дорівнює 16, 18 електронам (знак -2 вказує на те, що в ньому на два електрони більше, ніж число протонів), 17 нейтронів і масове число, що дорівнює 33.
Атом Н має 21 протон, атомний номер дорівнює 21, 18 електронам (знак +3 вказує, що у нього на три менше електронів, ніж число протонів), 27 нейтронів і масове число, рівне 48.
Мені Діого Лопес Діас
Джерело: Бразильська школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-atomo.htm


