Теорія гібридизації виникла як доповнення до Теорія октетів, зумівши пояснити будову більшої кількості молекул, включаючи молекули, утворені бором (В).
Цей елемент має п’ять електронів основного стану з наступною електронною конфігурацією:
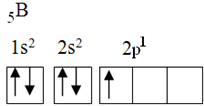
Згідно з теорією октету, бор міг утворити лише один ковалентний зв’язок, оскільки він має лише одну неповну атомну орбіталь. Однак експериментально зазначається, що цей елемент утворює сполуки, в яких він виконує більше одного зв’язку.
Прикладом є трифторид бору (BF3). Як показано нижче, бор утворює три ковалентні зв’язки з фтором, розділяючи три пари електрони і мають шість електронів в останній оболонці (валентний шар), тобто виняток з правила октет.
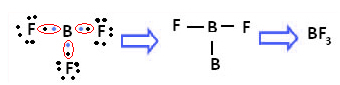
Це пояснюється явищем гібридизації, яке відбувається з бором. Виявляється, електрон з підрівню 2s поглинає енергію і переходить у збуджений стан, в якому перескакує на порожню орбіталь підрівню 2р. Таким чином утворюються три неповні орбіталі, які тепер можуть утворювати три ковалентні зв’язки:
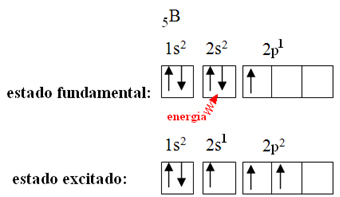
Однак зв’язки, утворені в трифториді бору, однакові, але якщо подивитися вище, то є два зв’язки різні, оскільки один з них буде зроблений за допомогою орбіталі s, а інші два - за допомогою орбіталі цього типу. тип p. Тут відбувається гібридизація, тобто неповні орбіталі зливаються, породжуючи три
гібридні орбіталі або гібридизований, які ідентичні та відрізняються від оригіналів: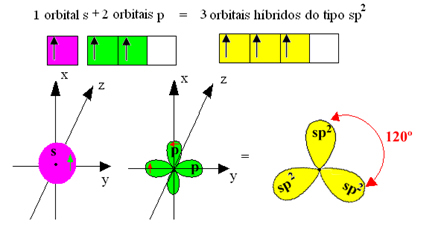
Оскільки ці гібридні орбіталі складаються з однієї s-орбіталі та двох р-орбіталей, ця гібридизація називається sp² гібридизація.
Фтор, який зв’язується з бором, має дев’ять електронів. Його електронний розподіл та орбіталі наведені нижче:
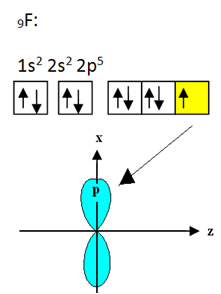
Зверніть увагу, що кожен атом фтору може утворювати лише один ковалентний зв’язок і що орбіталь, що утворює цей зв’язок, має тип p. Отже, спостерігайте нижче, як формуються орбіталі при встановленні зв’язків, що утворюють BF3 і подивіться, як посилання ідентичні, наприклад σp-sp2:
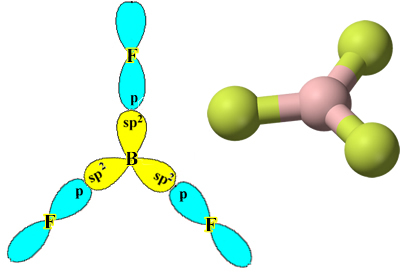
Це також трапляється з іншими елементами, див., Наприклад, текст “Гібридизація берилію”.
Дженніфер Фогача
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/hibridizacao-boro.htm


