Алюміній отримують в результаті металургійних процесів. Металургія - це область, яка вивчає перетворення руд у метали або металеві сплави. Цим методом отримують кілька металів, такі як мідь, титан, залізо та марганець.
У випадку алюмінію основною рудою, що використовується, є боксит (рисунок), який містить гідратований оксид алюмінію (Aℓ2О3. х Н2О) та різні домішки.

В металургії алюмінію відбуваються наступні чотири етапи:
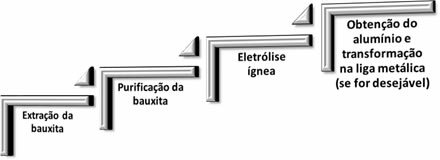
Коли оксид алюмінію (Aℓ2О3 (s)) відокремлюється від бокситу, його назва стає глинозем.
Раніше було зроблено наступне: глинозем обробляли соляною кислотою з отриманням хлориду алюмінію; який поміщали в реакцію з металевим калієм або натрієм, викликаючи відновлення сполуки і даючи металевий алюміній:
Aℓ2О3 (s) + 6 HCℓ(тут)→ 4 AℓCℓ3 (вод.) + 3 год2О(ℓ)
ACℓ3 (вод.) + 3K(s)→ 3 KCℓ(s) + Aℓ(s)
Однак цей спосіб був дуже дорогим і неефективним, тому алюміній вважався рідкісним металом.
Але в 1886 р. Два вчені окремо розробили згаданий вище метод, при якому використовувався магматичний електроліз. Цими вченими був американець Чарльз М. Холл і француз Поль Еро, тому цей метод і став називатися
Процес Холла-Еро або просто,Процес Холла, тоді як Чарльз М. Хол запатентував його.Ключовим моментом, який вони виявили, було те, як зробити рідину з оксиду алюмінію для цього. мати можливість проводити свій магматичний електроліз, оскільки проблема полягала в тому, що його температура плавлення була вище 2000 ° С. Вони використовували флюс, кріолітову руду (Na3AℓF6), який зміг знизити температуру плавлення оксиду алюмінію приблизно до 1000 ° С.
Таким чином, як показано на діаграмі нижче, цю суміш оксиду алюмінію та кріоліту помістили в сталеву електролітичну посудину, покриту вуглецем. Через цю розплавлену суміш проходить електричний струм. Стінки контейнера, які контактують із сумішшю, діють як негативний полюс електролізу (катод), де відбувається відновлення катіонів алюмінію. Анодом (позитивним полюсом) є балони з графіту або вуглецю, тобто обидва з вуглецю, де відбувається окислення аніонів кисню:
Напівреакція катода: 4 Aℓ3+(ℓ) + 12 і- → 4 Aℓ(ℓ)
Напівреакція анода: 6 O2-(ℓ) → 12 і- + 3 O2 (г)
Утворений кисень реагує з вуглецем в аноді, а також утворює вуглекислий газ:
3 O2 (г) + 3 С(s) → 3 CO2 (г)
Отже, загальна реакція та схема цього магматичного електролізу, що призводить до появи алюмінію, визначається:

Отриманий алюміній знаходиться у рідкій формі, оскільки його температура плавлення становить 660,37 ºC, тобто нижче, ніж у суміші глинозему та кріоліту. Алюміній також щільніший за суміш, і тому він осідає на дні ємності, де збирається.
При виробництві 1 тонни алюмінію використовується:
- Від 4 до 5 тонн бокситів, звідки про 2 тонни глинозему;
- 50 кілограмів кріоліту (Природних запасів кріоліту не так багато, тому його зазвичай отримують шляхом його синтезу з флюориту (CaF2), мінерал, найпоширеніший у природі);
- 0,6 т вугілля для електродів.
Щорічно виробництво алюмінію перевищує 27,4 млн. Тонн.
Серед основних алюмінієвих сплавів ми маємо наступне:

Дженніфер Фогача
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/obtencao-aluminio-por-meio-eletrolise.htm

