До функції азоту є групою органічні сполуки які мають атоми азот приєднаний до вуглецевого ланцюга. Вони розрізняються відповідними функціональними групами, які є наборами атомів, з’єднаних у певній конфігурації та які визначають характерні властивості кожної функції.
Функції азоту:
аміни;
аміди;
нітросполуки;
нітрили;
ізонітрили.
Читайте також:Які функції виконує кисень?
Короткий опис функцій азоту
Функції азоту — це органічні сполуки, які містять атомів азоту.
Аміни, аміди, нітросполуки, нітрили та ізонітрили є функціональними групами азоту.
Неорганічні функції розрізняють за функціональною групою.
Аміни отримують шляхом заміщення водні аміаку алкільними радикалами.
Аміди мають однаковий атом вуглецю, з’єднаний з азотом і вуглецем. кисень.
Нітросполуки містять групу -NO.2.
Нітрили характеризуються наявністю потрійного зв'язку між вуглецем і азотом.
Ізонітрили мають потрійний зв’язок між азотом і вуглець, з азотом, приєднаним до вуглецевого ланцюга.
Відеоурок про функції азоту
Що таке функції азоту?
Функції азоту — це сукупність
органічні функції, які мають у своїй структурі атом нітрогену, крім атомів вуглецю та водню. Це: аміни, аміди, нітросполуки, нітрили та ізонітрили,Те, що відрізняє азотисті функції, - це відповідні функціональні групи, які є структурним розташуванням атомів, що відповідає за властивості речовини.
Які функції азоту?
аміни
Органічна функція шахта характеризується шляхом зв'язування принаймні одного вуглецевого ланцюга з атомом азоту. Функціональна група амінів -N-R1Р2Р3 (групи R є вуглецевими ланцюгами або атомами водню, принаймні один з яких є вуглецевим ланцюгом).

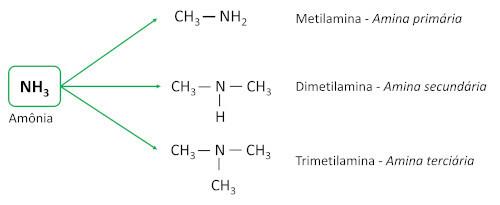
аміни отримують з аміаку (NH3), з одним або кількома атомами водню, заміненими атомами вуглецю або алкільними лігандами. Вони є основними речовинами, залишаючи в pH більше 7 у водному розчині.
Їх класифікують за кількістю атомів водню, заміщених вуглецевими лігандами (алкільними або арильними групами), які називаються заступниками.
- Первинні аміни: мають один вуглецевий замісник.
- Вторинні аміни: мають два вуглецеві замісники.
- третинні аміни: мають три вуглецеві замісники, тобто атом азоту більше не зв'язаний з жодним атомом водню, встановлюючи три Зв'язки прості з атомами вуглецю.
А номенклатура амінів дотримується вказівок IUPAC (Міжнародний союз теоретичної та прикладної хімії). У разі первинних амінів конструкція назви враховує кількість атомів вуглецю (префікс), характер зв’язку між атомами вуглецю (інфікс) і використовується термін шахта для суфікса (кінець слова).

Дивіться приклад:
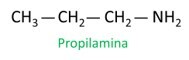
Призначаючи номери вуглецю для розташування радикалів, присвоюйте найменший можливий номер атому, найближчому до групи NH.2.
Для вторинних і третинних амінів номенклатура враховує найдовшу групу замісників, приєднану до азоту як основний ланцюг, а інші ліганди пишуться з префіксом, що вказує на кількість атомів вуглецю, і суфіксом -іл, з літерою N перед ними.

приклад:
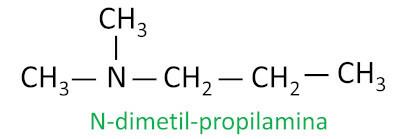
Аміди
Органічна функція амід характеризується зв'язування карбонільної групи (C=O) з атомом азоту, де азот може бути зв’язаний з атомами вуглецю або водню.
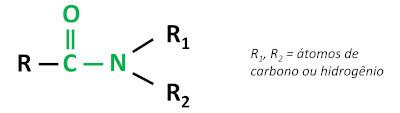
аміди є основними речовинами, залишаючи рН вище 7 у водному розчині. Речовина сечовина належить до групи амідів і є природною сполукою, присутньою в сечі, яка утворюється в результаті процесів розкладання, які відбуваються в живих організмах.
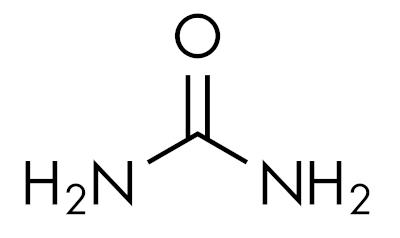
Аміди характерні залежно від рівня заміщення азоту. Подобається це:
- Первинні аміди: утримувати два атоми водню разом з азотом.
- Вторинні амідиабо однозаміщений: один із атомів водню замінено на вуглецевий ланцюг, тому азот підтримує одинарний зв’язок з воднем.
- третинні амідиабо переміщені: Нітроген більше не має водневих зв’язків, усі вони були замінені вуглецями.

Аміди є Названо згідно з IUPAC, молекули названі в послідовності:

У розгалуженому аміді атом вуглецю амідної групи бере участь в головному ланцюзі, і підрахунок вуглецю повинен починатися з нього. Подивіться:
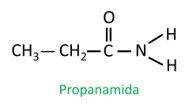 |
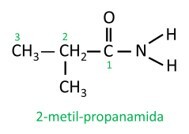 |
У однозаміщених або двозаміщених амідах літера N позначає положення гілки яка приєднана до атома нітрогену. Якщо в ланцюжку є інший радикал, він буде записаний після ідентифікації радикала, що відноситься до N.
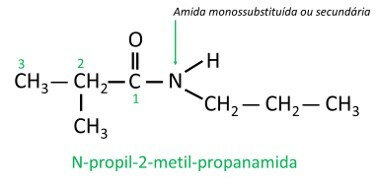
нітросполуки
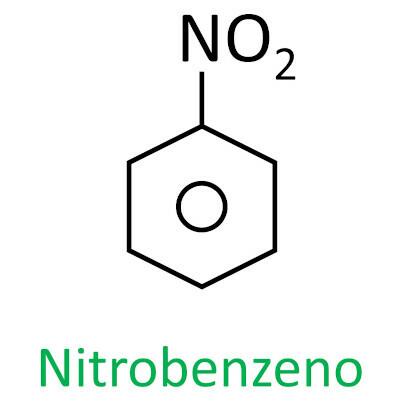
ви нітросполуки є органічними сполуками, які містять нітрогрупу (-NO2), приєднаний до вуглецевого ланцюга, який може бути аліфатичним (відкритим або лінійним) або ароматичним.
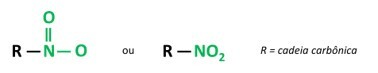
А Основною характеристикою цих речовин є їх вибухова сила. Вибухова здатність пов'язана з ароматичними нітросполуками, і чим більше число нітрогруп, тим сильніше вибух. Аліфатичні нітросполуки використовуються в лабораторіях як органічні розчинники.
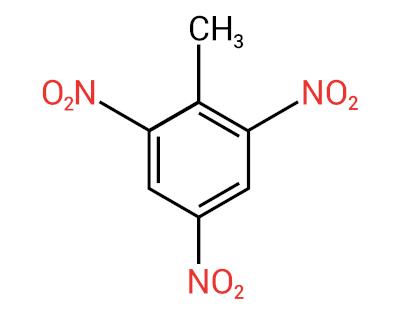
Номенклатуру цих сполук утворює слово нітро а потім ім'я вуглеводень (префікс + інфікс + закінчення -О).
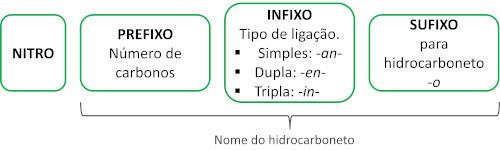
Подивіться кілька прикладів:
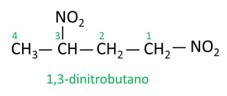 |
 |
нітрили
Нітрили — органічні сполуки, що характеризуються потрійний зв'язок між атомом Карбону та атомом Нітрогену, представляючи функціональну групу – C ≡ N. У нітрилах азот знаходиться на кінці, а вуглець приєднаний безпосередньо до вуглецевого ланцюга.

нітрили Також відомий як ціаніди, оскільки вони походять від реакцій із синильною кислотою (HCN).
вони є речовинами токсичний для людини, тому що в організмі вони можуть утворювати синильну кислоту при контакті зі шлунковою кислотою, запобігаючи процесам клітинне дихання клітин.
У природі нітрили можна знайти в деяких кісточкових плодах, але в дуже низькій концентрації, що не становить ризику, і в листі дикої маніоки.

Правило Iupac для номенклатури нітрилів визначає цей термін нітрил додавати як суфікс:

Подивіться кілька прикладів:
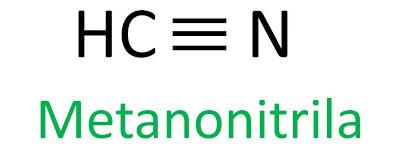 |
 |
Звичайною формою номенклатури для нітрилів є ціанід + радикальна назва.
ізонітрили
Ізонітрили, або ізонітрили, — сполуки, утворені в потрійний зв'язок між атомом Карбону та атомом Нітрогену, представляючи функціональну групу – R ≡ C. В ізонітрилах вуглець знаходиться на кінці, а азот приєднаний безпосередньо до вуглецевого ланцюга.

Ізонітрили відрізняються від нітрилів положенням атомів азоту і вуглецю, а також В ізонітрилах азот характеризується як гетероатом., оскільки він розташований між двома вуглецями.
Вони є нестабільними видами і можуть перетворюватися на нітрили при підвищених температурах. Реакції ізоціанідової кислоти призводять до утворення ізонітрилів, тому ці сполуки також відомі як ізоціаніди.
Молекули ізонітрилу дотримуються правила Юпака для назви:
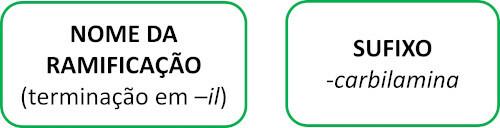
Подивіться кілька прикладів:
 |
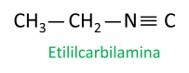 |
Застосування функцій азоту
Речовини, що належать до азотистих функцій, мають численні застосування, головним чином у промисловій сфері, для виробництва полімери, каучук, синтетичні волокна, фармацевтичні препарати, агрохімікати, пестициди та вибухові речовини.
До аміни використовуються у виробництві барвників, мило, ліки, в процесі вулканізація гуми, вибухові речовини та інші промислові процеси, а також містяться в рослинах і утворюються в процесі розкладання органічних речовин.

До аміди знайшли широке застосування в промисловості та хімічному секторі, які присутні у виробництві полімерів (таких як нейлон і поліуретан), смол, вибухових речовин, добрива, засоби від комах, добрива та препарати.

ви нітросполукиЙого основне застосування — виготовлення вибухових речовин. які використовуються у військовій, промисловій та металургійній сферах (для видобутку сировини). Однією з найвідоміших нітросполук є тринітротолуол, широко відомий як тротил. Інші застосування нітросполук у виробництві пестициди, бактерициди, барвники, переробка нафти тощо.

До нітрили використовуються як органічні розчинники в лабораторії та промисловості, беручи участь у процесах видобутку та виробництва деяких синтетичних волокон, пластикових полімерів, барвників та добрив.

До ізонітрили використовуються в різних процесах виробництва органічних сполук, таких як розчинники, і беруть участь у виробництві агрохімікатів, пестицидів, гуми та пластмас.
Читайте також:Галогеніди — речовини, які мають атоми галогенів, приєднані до карбонового ланцюга
Розв’язували вправи на функції азоту
питання 1
(FPS-PE-модифікований) Застосування азотистих сполук у синтетичній органічній хімії є дуже різноманітним і включає приготування ліків, барвників, вибухових речовин і вітамінів. Подивіться на сполуки нижче.
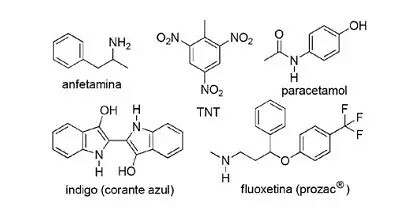
Про ці сполуки позначте неправильне твердження.
а) тротил — нітросполука.
b) Азотиста частина флуоксетину є вторинним аміном.
в) Амфетамін класифікується як первинний амід.
г) Індиго має у своїй структурі гетероароматичні кільця.
д) Азотиста частина парацетамолу є амідом.
роздільна здатність:
Літера С
предмет The є правильним, тому що тротил є нітросполукою, тому що в ньому немає груп2.
предмет Б правильно. Азотиста частина флуоксетину є вторинним аміном, оскільки вона пов’язана з двома вуглецевими сегментами.
предмет w є неправильним, оскільки амфетамін класифікується як первинний амін, а не амід. Зверніть увагу, що нинішня група - це NH2. Отже, це суть питання.
предмет d це правильно, оскільки індиго має у своїй структурі гетероароматичні кільця, тобто кільця, утворені атомами вуглецю та іншого елемента — в даному випадку азоту.
предмет Це є це правильно, тому що парацетамол є амідом, який містить вуглець, пов’язаний з азотом і киснем.
питання 2
(UFMS) Йерба мате (Ілекс парагуарський), родом з Південної Америки, використовується як тонізуючий і стимулюючий напій. Для приготування можна використовувати продукт, отриманий в результаті обробки листя йерба мате chimarrão і tereré, серед інших напоїв, які зазвичай і культурно споживаються в регіонах Аргентини, Парагваю та Бразилія. Великий інтерес до йерба мате викликаний присутніми хімічними сполуками, завдяки його антиоксидантним, стимулюючим і сечогінним властивостям.
(Доступний у: http://repositorio.utfpr.edu.br/jspui/bitstream/1/3158/1/PG_PPGEP_Henrique%2C%20 Flavia%20Aparecida_2018.pdf. Дата доступу: 01 лист. 2018. Адаптований).
Стимулюючі властивості йерба мате пов’язані з вмістом у ньому метилксантинів, одним із основних з яких є кофеїн, структуру якого наведено нижче:

Аналізуючи структурну формулу кофеїну, можна стверджувати, що він має такі органічні функції та властивості:
а) альдегідні та амідні, основні.
б) амін і амід, лужний.
в) амін і кетон, лужні.
г) кетон і амід, амфотерний.
д) карбонова кислота й амін, основні.
роздільна здатність:
Літера Б
Аналізуючи структуру кофеїну, можна ідентифікувати амінну та амідну функціональні групи, як показано на зображенні нижче. Оскільки ці дві групи мають основні або лужні характеристики, кофеїн також має цю характеристику, тобто водні розчини кофеїну мають pH вище 7.
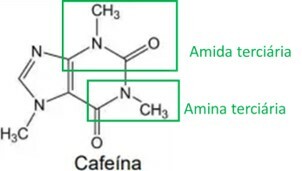
Ана Луїза Лоренцен Ліма
Вчитель хімії
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/funcoes-nitrogenadas.htm

