THE Закон швидкості реакції пов'язує швидкість хімічного перетворення з концентрацією реагентів у кількості речовини (моль / л), яку можна зазначити наступним чином:

Наприклад, розглянемо таку загальну реакцію:
aA + bB → cC + dD
Скажімо, ми збільшуємо концентрацію реагентів А і В, що буде зі швидкістю реакції? Ну, оскільки кількість частинок реагенту буде збільшуватися в тому самому просторі, між ними відбуватимуться більш ефективні зіткнення, що призведе до збільшення швидкості розвитку реакції. А це означає, що це збільшить вашу швидкість.
Тому швидкість реакції прямо пропорційна концентрації реагентів. Однак це залежить і від температури. Отже, ми маємо таке математичне рівняння, яке представляє закон швидкості реакції:

Про те, що:
v = швидкість реакції;
k = константа, яка залежить лише від значення температури;
α та β = показники ступеня, визначені експериментально.
Тільки тоді, коли реакція елементарна, тобто вона відбувається за один крок, показники в рівній мірі дорівнюють коефіцієнтам збалансованого хімічного рівняння:
v = k. [THE]. [B]B. Однак в інших випадках відповідну ефективність, до якої повинна бути підвищена концентрація кожного реагенту, слід визначати експериментально.Закон швидкості реакцій називається багатьма назвами, ось кілька: Закон масових дій, Рівняння швидкості, Кінетичний закон реакції та Закон Гульдберга-Вааге.
Розглянемо приклад того, як застосовувати цей закон:
Розглянемо таку елементарну реакцію:
2 HCl (g) → H2 (г) + Кл2 (г)
а) Напишіть рівняння швидкості цієї реакції;
б) Шляхом експериментів швидкість цієї реакції розкладання хлористого водню та концентрація цього реагенту при постійній температурі 25 ° C були зазначені в таблиці нижче:
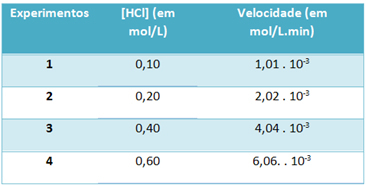
Виходячи з цього, визначте характерну константу швидкості цієї реакції при згаданій температурі.
Дозвіл:
The) v = k. [HCl]2
б) v = k. [HCl]2
k = __v___
[HCl]2
k = 1,01. 10-3 моль. L-1. хв-1
0,01 моль L-1
k = 1,01. 10-1 хв-1
Для розв’язання літери “b” можна використовувати дані будь-якого з експериментів про те, що отримане значення буде однаковим.
Але що, якщо реакція не елементарна? Як можна буде вирішувати подібні питання в не елементарних реакціях? Щоб дізнатись як, прочитайте Закон швидкості для неелементарних реакцій.
Дженніфер Фогача
Закінчив хімію
Джерело: Бразильська школа - https://brasilescola.uol.com.br/quimica/lei-velocidade-das-reacoes-quimicas.htm

